解冻背景
温度敏感细胞疗法正在改变临床治疗方式,使得持续的冷链管理对于向患者提供治疗至关重要。从血液成分分离采集到临床,由于制备成品细胞疗法涉及多步骤流程,且给药时间和地点存在不可避免的不确定性,因此控制低温生物学储存条件变得复杂。研究发现,在低于 -120°C 下冷冻保存治疗药物可在细胞库中实现稳定、长期的储存,直至需要治疗为止。1–3
冷链管理包括三个关键阶段:
- 冷却
- 存储*
- 解冻1,3–5
对于临床细胞系统,前两个阶段通常使用经过验证的方案和自动控速冷冻机进行精确控制和记录。1,6对于临床细胞系统,前两个阶段通常使用经过验证的方案和自动控速冷冻机进行精确控制和记录。1,7
高效解冻对细胞活力和性能影响最小,是流程的关键环节,通常是在即时诊断进行的最后操作。此类治疗有可能挽救生命,但如若在解冻过程中出现错误,可能影响治疗效果,从而对患者造成严重影响,同时给产品开发者带来高昂成本和声誉受损。
高效解冻对细胞活力和性能影响最小,是流程的关键环节,通常是在即时诊断进行的最后操作。此类治疗有可能挽救生命,但如若在解冻过程中出现错误,可能影响治疗效果,从而对患者造成严重影响,同时给产品开发者带来高昂成本和声誉受损。1,5,8,9冷冻保存和解冻在工作流程的多个步骤发生(图 1),应尽可能减少由这些过程造成的任何有害影响。
本指南总结了按照传统慢速冷冻方法解冻的科学原理。我们探讨了细胞解冻如何从历史发展演变为当今使用的新技术,以及关键指标和组成部分(如升温速率和冰晶结构)的物理和生物学影响。此外,本指南还包含对科学文献中关键研究的综述,以及对冷却与升温速率之间相互作用的考虑,这些内容适用于细胞疗法和基因疗法。我们不考虑无冰冷冻保存(有时称为“玻璃化”),这是一种不适合大多数细胞疗法和冷冻袋的专用方法。
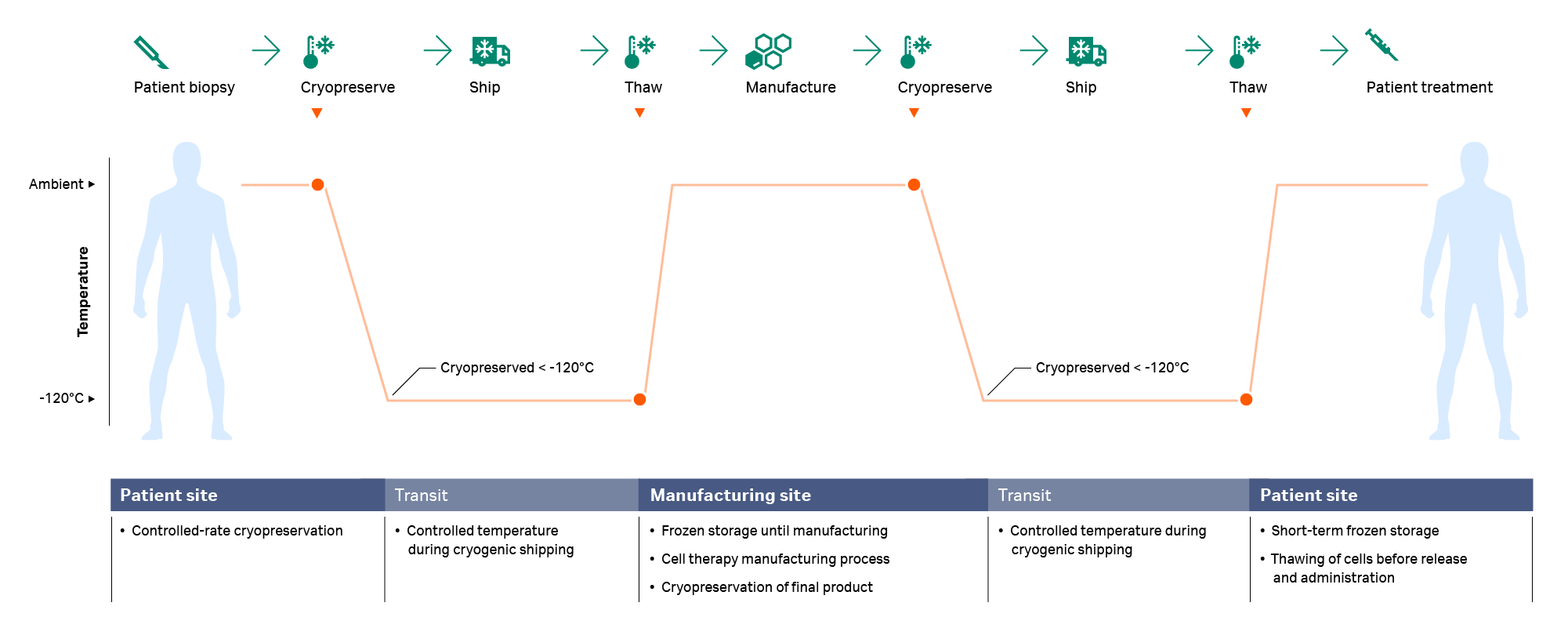
图 1.典型的冷冻链——解冻步骤通常在细胞疗法制备过程中发生两次:一次是在起始材料到达制备地点后,另一次是在输注前。
解冻的历史——为何我们采用当前方法
冷冻保存材料的解冻过程历来采用相对简单的程序,且存在较强的主观性。通常,将冷冻样本浸入 37°C 水浴中,肉眼判断最后一块冰何时融化(湿解冻)。6,10该方法简单、经济且成熟,但需专业技术人员操作才能确保成功与一致性。使用者行为及实验室环境的差异可能导致批次间产品温度管理的差异。未经培训的操作人员可能选择略微不同的、且常具主观性的冷冻袋角度、搅拌速度及解冻结束标准,从而产生一系列不一致的结果。
临床现场并不总是有专门的技术人员进行解冻,特别是当为了降低风险而需要分多次剂量(多个冷冻袋)进行治疗时。因此,在患者现场解冻越来越多地由临床工作人员进行,而这些人员可能缺乏冷冻保存的培训和经验,11,从而增加处理不当的风险、降低细胞活力并损害治疗效果。
尽管水浴在研究环境中已经足够,但在临床和洁净室环境中却存在固有困难。除工艺和产品变化的风险外,温水还会带来受控环境下不可接受的污染风险。12–14还需具备用于灭菌、复温、再填充和温度稳定的时间和设施。
为应对这些限制,能够处理冷冻袋中较大样本量的无水解冻装置逐渐受到青睐。1,5,15–18这些系统消除了使用者间差异,提供一致且可编程的流程,最大限度减少使用者主观干预,包括计算机控制、监测和数据记录等选项。研究表明,干式解冻也可成功应用于非细胞治疗材料(如血浆)1,15–18,从而进一步推动了这些设备的广泛应用。
解冻速率的科学原理
控制冷却以实现稳定解冻:冷却和解冻速率本质上相互关联,考虑其中一个无法脱离另一个。历史上,低温生物学家认为快速解冻对于成功细胞回收至关重要。19–21然而,随着近年来的技术发展,这一教条已被推翻,并且仅适用于细胞疗法不可接受的极快冷却速率。1,4关于升温仍存在许多误区,可能出于以下原因:
- 缺乏积极研究:关于哺乳动物体细胞的最后一项系统性研究发表于 1979 年,距今已超过 30 年。22,同一时期关于冷冻保存精子升温速度的论文至少有 6 篇,关于冷冻保存胚胎升温速度的论文至少有 5 篇。
- 对现有数据的误用:人们一直认为精子和胚胎的数据可转化用于体细胞。
- 解冻后延迟清洗细胞:DMSO毒性可在DMSO被洗掉之前损害解冻后的细胞。一些程序将细胞的物理升温与清洗视为一个“解冻”步骤。延迟清洗有时会与缓慢解冻相混淆。
在实验室中,约 2 至 3 分钟的湿解冻过程操作便捷;然而,当解冻以精确控制速率冷却的体细胞时,不需要这种快速方法。研究人员已针对多种细胞类型测试了缓慢冷却后较慢的升温速度,结果表明,对肝细胞23、神经细胞24、神经细胞4、神经细胞25、L 细胞22、未处理的单采血样5和淋巴细胞26的解冻后结果均无影响。令人惊讶的是,尽管普遍认为快速升温有利,但尚无研究表明细胞治疗过程/免疫疗法需要快速解冻。
人们通常认为,为防止冰在升温过程中重新结晶,需要快速融化。上述研究表明,只要适当控制冷却,无论升温速度如何,冰都不可能重新结晶。
冷却过程中的冰晶形成:在冷却过程中,冰晶在成核时形成并通过系统发展——最初以小型树枝状晶体形式出现,物理上表现为相互交织且方向各异的针状结构。随着冷却的进行,水分子附着于冰晶,单个晶体的尺寸不断增大。这一过程导致细胞外渗透浓度升高,进而导致细胞脱水。如果冷却速度缓慢,为每分钟几摄氏度或更低,晶体就有足够的时间完全形成,并且在解冻时无法重新结晶。
当冷却速度过快时,可能会出现问题,包括细胞损伤。4快速冷却后,水分子没有足够的时间附着到冰晶上或从细胞中流出。当温度达到玻璃化转变温度(约 -120°C)且不再可能发生分子运动时,晶体会以悬浮状态存在,结构不稳定。3然后,当系统升温并于解冻时重新引入热量,水分子开始再次附着于冰晶。28这一现象称为重新结晶,会对细胞施加显著渗透压力并导致损伤。
幸运的是,冷冻保存细胞疗法和哺乳动物体细胞所需的缓慢冷却速度(每分钟最高几度)可形成热力学稳定的冰晶,从而无需快速升温。4 这一过程可在不同冷却速率下冷却和解冻时通过低温显微镜在冰晶上观察到(图 2),并且已发现与细胞回收结果相关。
一项近期低温显微镜研究表明,细胞活力丧失与升温过程中冰晶结构的变化相关。4在高冷却速度 (-10°C/min) 下,冰晶结构呈现高度无定形状态。随后在较长时间(15 分钟或更久)内解冻时,观察到冰重新结晶现象,表明冷冻细胞受到机械性破坏。以更典型的 -1°C/min 速率冷却时,缓慢升温过程中冰晶结构无变化。相比之下,在水浴中两分钟内从 LN2 温度升温,升温速度约为 100°C/min。而持续 10 分钟的稳态升温(干式解冻设备典型处理时长)平均升温速率为 20°C/min。这两种方法均远快于受控冷却速率,且相较于物理和生物学推荐的标准,被视为快速。4
不同体积的冷冻袋样本以 -1°C/min 左右的速率进行干式解冻,虽可能比传统水浴解冻耗时更长,但可获得相当的解冻后细胞产量,并消除水浴湿式解冻带来的不一致风险。

图 2.冷冻保存过程中拍摄的低温显微镜图像,显示了冰在冷却和升温过程中如何发生变化。标记为蓝色的样本冷冻保存速度非常快,因此在储存温度下冰未完全形成(蓝色图像 #2)。在蓝色图像 #5 之后,冰晶结构在解冻过程中发生变化(有时称为重新结晶)。相反,以受控方式冷却的细胞(橙色图像 #1-#4)有足够的时间在冷却时形成较大冰晶,因此在升温时不会观察到重新结晶(橙色图像 #5)。4冰重新结晶发生在升温阶段,而非冷却阶段——橙色图示显示了如何在冷却过程中对冰进行优化控制,以防止升温时发生变化。
解冻后毒性:除避免冰晶结构变化外,尽量减少冷冻保护剂的毒性也很重要。在冷冻保存过程中,会添加冷冻保护化学物质来保护细胞免受损害,其中 DMSO 是用于此目的的最常用物质。在液态下,这些化学物质对细胞具有毒性29,30,且毒性在较高温度下更为显著。在冷冻过程之前,在高于冰点几度的低温下添加冷冻保护剂可最大限度地降低毒性30–32;然而,随着解冻和温度升高,毒性效应会再次出现。
解冻后冷冻保护剂的毒性在冷冻保存周期的所有液相阶段均具有相同的破坏潜力,但常被忽视。由于细胞已受到冷冻/解冻周期的应激,因此在解冻时对冷冻保护剂毒性的敏感度至少与在冷却时同样敏感,甚至更敏感。30–32一定的缓冲时间仍可接受,但因产品而异。例如,市售 Kymriah™ 和 Yescarta™ CAR-T 疗法的制造商建议,在室温(20°C-25°C)下将细胞在冷冻保护剂中解冻后,分别在不超过 30 分钟和 3 小时内将细胞输注到患者体内。33–34 这一时间限制包括输液期间的任何中断时间,有助于确保维持最大细胞活力。
在水浴中解冻时间过长可能对细胞回收产生不利影响,因为水的高热传导性会使样本迅速升温至 37°C。这种快速升温过程会在袋内产生较大温度梯度——部分区域(尤其是接头周围)可能仍残留小冰晶,而其他区域已达到水浴温度。湿式解冻的缓解策略包括在加热过程中搅动袋子,并在所有冰融化之前将其从水浴中取出。然而,此类措施因使用者而异,且容易出现样本和批次间差异。干式解冻系统通过自动化和更慢的解冻速度,有助于减轻细胞冷冻保护剂损害并提高解冻过程间的一致性。
细胞解冻后预期会发生什么
从解冻系统中取出细胞并洗去冷冻保护剂溶液(如适用)标志着冷冻保存周期结束。冷冻保存是一个复杂的过程,可能对细胞产生严重影响。为了正确理解整体生物系统的影响,需考虑解冻后时间对细胞损伤的影响,如图 3 所示。
冷冻保存周期的某些影响可立即观察到,而其他影响则需要时间来显现。这一时间因素是细胞疗法广泛应用的一项关键考虑因素。冷冻保存后的细胞死亡可按类型分层:坏死性死亡和凋亡。
坏死性死亡包括在冷冻保存过程中立即杀死的细胞(在大多数细胞活力检测中显示为解冻后膜通透性细胞),以及从系统中完全丢失的细胞,无论是通过洗脱步骤还是完全裂解。这些“缺失”的细胞通常不会出现在活力检测中,因为它们已从系统中去除,但可以通过冷冻前和解冻后的细胞数量差异检测到。35–36
由凋亡引起的细胞死亡可能在解冻后数小时至 2-3 天内发生(图 3),因此在冷冻保存完成后立即测量细胞活力可能会产生不准确的阳性结果。这些细胞遭受亚致死性损伤,若损伤无法修复将发生凋亡。将细胞从细胞培养环境中取出也会降低其功能和代谢率。这种现象在冷冻保存结束后会变得明显,因此我们建议在解冻后不仅要检测细胞数量和活力,还应进行特定的功能性检测。
解冻后台盼蓝染色检测快速、简便、成熟且成本低廉。37该染料有助于确定细胞膜通透性,这与细胞死亡密切相关;然而,功能性死亡的细胞在检测时仍可能保持完整膜结构,从而导致假阳性结果。36台盼蓝也可用于细胞计数,以确定真实的活细胞数量。36
其他简单检测包括基于还原的测定,其中使用荧光素二乙酸酯、alamarBlue™ 试剂、PrestoBlue™ 试剂和 MTT(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑)等标记物来测定细胞代谢活性。38这些测定法更准确且对假阳性结果的敏感性较低,但它们通常需要一段孵育期,这增加了该过程的复杂性。3
更复杂的检测方法包括增殖检测、凋亡标志物检测以及针对细胞在体内预期用途的功能性测定,例如 NK 或 T 细胞靶向作用于表达特定标志物癌细胞的能力。35理想情况下,细胞活力和活性检测应在患者给药前进行,但在临床中这通常难以实现。因此,必须充分了解即时活力检测的局限性。
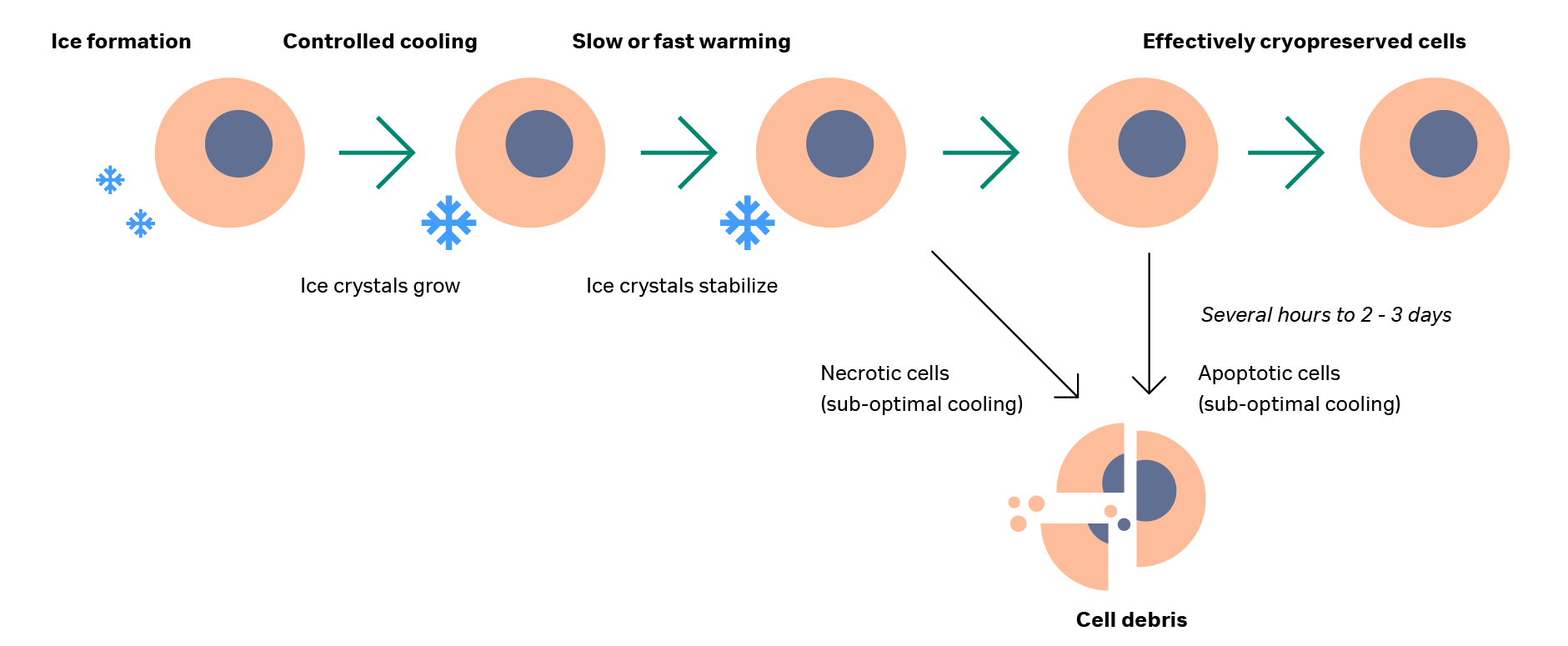
图 3.冷却、解冻期间和解冻后的细胞示意图。冰晶在细胞周围形成并在受控冷却过程中膨胀,在缓慢和快速解冻过程中均保持稳定。解冻后,部分细胞会受损并形成细胞碎片,而另一些细胞则会在解冻后数天内发生凋亡。剩余的细胞将存活下来,并被有效冷冻保存。
总结和结论
过去,解冻是冷冻保存周期中控制最不严格且一致性最差的步骤。近年来,干式解冻系统已问世,可减少与非受控过程及污染相关的问题,从而实现细胞疗法解冻的一致性和优化。
目前对冰晶结构及其在冷却和升温过程中变化的科学原理也有了更深入的理解。缓慢且精确控制的冷却过程虽对细胞疗法至关重要,但也允许更广泛的可接受解冻速度范围。
在评估解冻后的细胞活力时,务必确保使用适当的检测方法,同时考虑这些检测方法的稳健性以及治疗实用性。
总之,这些进展推动了更可控、更精准且一致的解冻过程,从而为患者提供更可靠的有效疗法。
了解如何使用 Cytiva 的冷冻解决方案简化您的细胞治疗过程并实现其标准化
* 包括在超低温下运输,对于基于 DMSO 的系统,通常定义为低于 -120°C,即玻璃化转变温度。
参考文献
- Hunt CJ. Technical considerations in the freezing, low-temperature storage and thawing of stem cells for cellular therapies. Transfusion Medicine and Hemotherapy. 2019;46(3):134-50.
- Fuller BJ, Lane N, Benson EE. Life in the frozen state: CRC press; 2004.
- Meneghel J, Kilbride P, Morris JG, Fonseca F. Physical events occurring during the cryopreservation of immortalized human T cells. PloS one. 2019;14(5):e0217304.
- Baboo J, Kilbride P, Delahaye M, Milne S, Fonseca F, Blanco M, et al. the Impact of Varying Cooling and thawing Rates on the Quality of Cryopreserved Human peripheral Blood t Cells. Scientific reports. 2019;9(1):3417.
- Water-free vs water bath cell thawing. Cytiva App Note. 2019.
- Kilbride P, Meneghel J. Freezing Technology: Control of Freezing, Thawing, and Ice Nucleation. Cryopreservation and Freeze-Drying Protocols: Springer. p. 191-201.
- Ericsson C, Franzén B, Nistér M. Frozen tissue biobanks. Tissue handling, cryopreservation, extraction, and use for proteomic analysis. Acta Oncologica. 2006;45(6):643-61.
- Guest RD, Rothwell DG, Kirillova N, Mowbray S, Sheard V, Gibbons S, et al. 059 Role of cryopreservation in the clinical delivery of T cell based adoptive cell therapies (ACT). Cryobiology. 2013;67(3):414.
- Workflow for primary human NK cell isolation,xeno‑free expansion, harvest, and cryopreservation. Cytiva App Note. 2019.
- Li R, Johnson R, Yu G, Mckenna DH, Hubel A. Preservation of cell-based immunotherapies for clinical trials. Cytotherapy. 2019;21(9):943-57.
- Mfarrej B, Gaude J, Couquiaud J, Calmels B, Chabannon C, Lemarie C. Validation of a flow cytometry-based method to quantify viable lymphocyte subtypes in fresh and cryopreserved hematopoietic cellular products. Cytotherapy. 2020.
- Muyldermans G, De Smet F, Pierard D, Steenssens L, Stevens D, Bougatef A, et al. Neonatal infections with Pseudomonas aeruginosa associated with a water-bath used to thaw fresh frozen plasma. Journal of Hospital Infection. 1998;39(4):309-14.
- Lazarus H, Magalhaes-Silverman M, Fox R, Creger R, Jacobs M. Contamination during in vitro processing of bone marrow for transplantation: clinical significance. Bone marrow transplantation. 1991;7(3):241-6.
- F Lindholm P, Annen K, Ramsey G. Approaches to minimize infection risk in blood banking and transfusion practice. Infectious Disorders-Drug Targets (Formerly Current Drug Targets-Infectious Disorders). 2011;11(1):45-56.
- Röllig C, Babatz J, Wagner I, Maiwald A, Schwarze V, Ehninger G, et al. Thawing of cryopreserved mobilized peripheral blood—comparison between waterbath and dry warming device. Cytotherapy. 2002;4(6):551-5.
- Triana E, Ortega S, Azqueta C, Pomares H, Valdivia E, Duarte R, et al. Thawing of cryopreserved hematopoietic progenitor cells from apheresis with a new dry‐warming device. Transfusion. 2013;53(1):85-90.
- Heger A, Pock K, Römisch J. Thawing of pooled, solvent/detergent-treated plasma octaplasLG®: validation studies using different thawing devices. Transfusion Medicine and Hemotherapy. 2017;44(2):94-8.
- Baust JM, Corwin WL, Snyder KK, Baust JG, Van Buskirk RG. Development and Assessment of a Novel Device for the Controlled, Dry Thawing of Cryopreserved Cell Products. BioProcessing. 2016;15(1):1538-8786.
- Shu Z, Heimfeld S, Huang Z, Liu C, Gao D. Progress in Cryopreservation of Stem Cells and Immune Cells for Cytotherapy. Progress in Stem Cell Transplantation: InTech; 2015.
- Fleck R, Fuller B. 21 Cell Preservation. Medicines from Animal Cell Culture: Wiley; 2007.
- Thompson ML, Kunkel EJ, Ehrhardt RO. Cryopreservation and Thawing of Mammalian Cells: Wiley; 2014.
- Akhtar T, Pegg D, Foreman J. The effect of cooling and warming rates on the survival of cryopreserved L-cells. Cryobiology. 1979;16(5):424-9.
- Kilbride P, Lamb S, Gibbons S, Bundy J, Erro E, Selden C, et al. Cryopreservation and re-culture of a 2.3 litre biomass for use in a bioartificial liver device. PloS one. 2017;12(8):e0183385.
- Drummond NJ, Dolt KS, Canham MA, Kilbride P, Morris GJ, Kunath T. Cryopreservation of midbrain dopaminergic neural cells differentiated from human embryonic stem cells. bioRxiv. 2020.
- Harris L, Griffiths J. Relative effects of cooling and warming rates on mammalian cells during the freeze-thaw cycle. Cryobiology. 1977;14(6):662-9.
- Thorpe P, Knight SC, Farrant J. Optimal conditions for the preservation of mouse lymph node cells in liquid nitrogen using cooling rate techniques. Cryobiology. 1976;13(2):126-33.
- Sahagian ME, Goff HD. Fundamental Aspects of the Freezing. Freezing effects on food quality. 1996;72:1.
- Morris GJ, Goodrich M, Acton E, Fonseca F. The high viscosity encountered during freezing in glycerol solutions: effects on cryopreservation. Cryobiology. 2006;52(3):323-34.
- Morris TJ, Picken A, Sharp DMC, Slater NKH, Hewitt CJ, Coopman K. The effect of Me2SO overexposure during cryopreservation on HOS TE85 and hMSC viability, growth and quality. Cryobiology. 2016;73(3):367-75. doi: https://doi.org/10.1016/j.cryobiol.2016.09.004.
- Elliott GD, Wang S, Fuller BJ. Cryoprotectants: A review of the actions and applications of cryoprotective solutes that modulate cell recovery from ultra-low temperatures. Cryobiology. 2017;76:74-91.
- Barcelo H, Faul J, Crimmins E, Thyagarajan B. A practical cryopreservation and staining protocol for immunophenotyping in population studies. Current protocols in cytometry. 2018;84(1):e35.
- TREE TI, ROEP BO, PEAKMAN M. Enhancing the sensitivity of assays to detect T cell reactivity: the effect of cell separation and cryopreservation media. Annals of the New York Academy of Sciences. 2004;1037(1):26-32.
- Kymriah Data Sheet - ANNEX 1 - SUMMARY OF PRODUCT CHARACTERISTICS. Novartis. 2019.
- Yescarta Data Sheet - ANNEX 1 - SUMMARY OF PRODUCT CHARACTERISTICS. Kite. 2019.
- Baust JG, Gao D, Baust JM. Cryopreservation: An emerging paradigm change. Organogenesis. 2009;5(3):90-6.
- Murray KA, Gibson MI. Post-thaw Culture and Measurement of Total Cell Recovery is Crucial in the Evaluation of New Macromolecular Cryoprotectants. Biomacromolecules. 2020.
- Strober W. Trypan blue exclusion test of cell viability. Current protocols in immunology. 1997;21(1):A. 3B. 1-A. 3B. 2.
- Bahsoun S, Coopman K, Akam EC. The impact of cryopreservation on bone marrow-derived mesenchymal stem cells: a systematic review. Journal of translational medicine. 2019;17(1):397.