电荷变体特征是生物制品上游和下游工艺开发中重要的分子特征属性。电荷变体表征可用于支持质量控制,以确保生物制品生产过程的一致性。在本研究中,我们描述了一种使用 DIGE 预标记技术、等电聚焦 (IEF) 电泳和 Amersham™ ImageQuant™ 800 系统进行多重荧光检测的电荷变体分析新方法。
样本和方法
本研究使用的样本是基于人 IgG Fc 片段的修饰抗体片段。每个片段(片段 1、2 和 3)都有不同的特征。片段 1 由单结构域 VH-Fc 融合蛋白组成。片段 2 和 3 由 Fc 融合蛋白组成。片段通过二硫键连接(表 1),从而形成同型二聚体或异型二聚体。同型二聚体片段对(1 和 2)单独表达或以异型二聚体对的形式表达,即片段 1 和 2 的组合,或片段 1 和 3 的组合。
每个样本均使用 CyDye™ DIGE fluor Cy™3 或 Cy™5 染料进行标记。样本标记通过标准 1D SDS-PAGE 在还原条件下进行检查。标记的蛋白质样本通过 IEF(第一维)分离,然后通过 SDS-PAGE(第二维)分离。预标记的样本分别加载至 7 cm pH 3-10 NL(非线性)和 24 cm pH 3-10 L(线性)Immobiline™ DryStrips,使用 DeStreak 再水化溶液(含 pH 3-10 NL 和 pH 3-10 L IPG 缓冲液)进行再水化。IEF 电泳使用 Ettan™ 仪器 IPGphor™ 3 等电聚焦装置进行。所有样本均在还原条件下运行。电泳后,使用 Amersham ImageQuant™ 800 Western 印迹成像系统和 Amersham Typhoon™ 生物分子成像仪捕获凝胶图像。捕获的图像数据通过 Melanie™ 9 2D 图像分析软件进一步分析。图 1 展示了从蛋白质标记到图像分析的整个工作流程。
表 1.本研究中分析的样本
| 样本 | 片段组合 | 理论分子量(Mr) | 理论 pI |
| A | 同型二聚体 | 片段 1 39 × 2 | 8.1 |
| B | 同型二聚体 | 片段 2* 47 × 2 | 6.4 |
| C | 1 和 3* | 39 和 47 | 8.1 和 6.5 |
| D | 1 和 2* | 39 和 47 | 8.1 和 6.4 |
* 已知片段 2 和 3 分别存在或不存在 O-糖基化位点,从而导致不同的翻译后修饰
图 1.本研究中使用的电荷变体分析工作流程。
1D SDS-PAGE
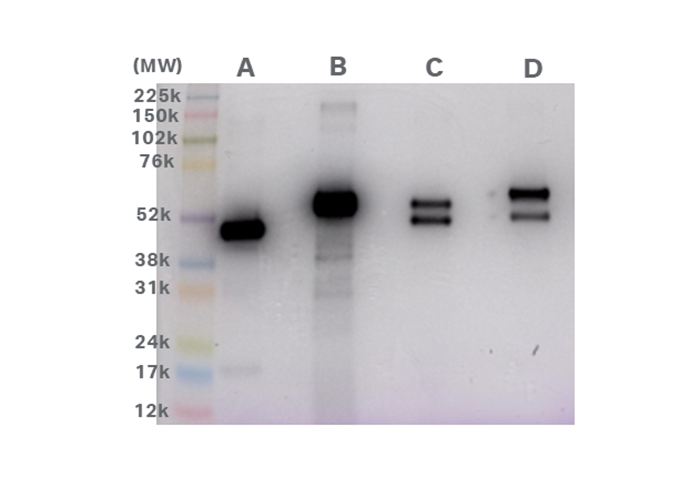
图 2 显示了使用 CyDye™ DIGE fluor Cy™5 染料预标记样本的 1D SDS-PAGE 结果。各样本中主要产物与表 1 所示的各片段表观分子量一致,但结果表明样本 A、C、D 中片段 1 的分子量存在一定差异(分子量 A < c="" />< d="" />< b)。此外,结果还表明片段="" 2="" 的表观分子量略高于片段="" />
图 2.使用 CyDye™ DIGE fluor Cy™5 染料预标记样本进行 1D SDS-PAGE。将 Amersham™ 彩虹标记剂添加至样本,并通过 Amersham ImageQuant™ 800 成像系统在 Cy™5 颜色标记模式下捕获图像。Cy™5 荧光信号(16 位灰度)和颜色标记的 RGB 图像叠加在一张图像上。
等电聚焦电泳
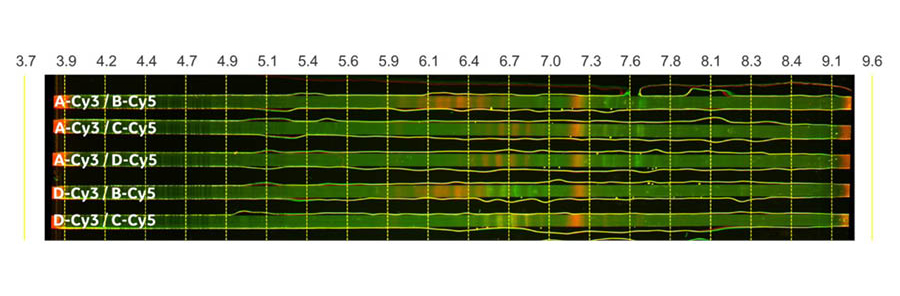
CyDye™ DIGE fluor Cy™3 和 Cy™5 预标记样本使用 24 cm pH 3-10 L(线性)Immobiline™ DryStrip 凝胶和 Ettan™ 仪器 IPGphor™ 3 等电聚焦装置进行 IEF 分离。IEF 分离后,使用 ImageQuant™ 800 成像仪在荧光模式下捕获 Immobiline™ DryStrip 凝胶上分离样本的 Cy™3 和 Cy™5 多重荧光图像(图 3)。
IEF 分离结果表明,每个片段都有数种电荷变体。片段 1 在 pH 6.5 至 7.8 范围内存在数种电荷变体,样本 B 中的片段 2 在 pH 5.9 至 6.5 范围内存在数种电荷变体。相比之下,样本 D 和 B(均包含从上至下第四条带中显示的片段 2)叠加效果不佳。这表明当片段 2 在不同片段组合表达时具有不同的电荷变体。样本 C 和 D 具有相似的电荷变体,这从其条带的紧密叠加模式(如从上至下第五条带所示)中可以看出。
图 3.通过 IEF 分离的样本对中电荷变体的组合。图像使用 ImageQuant™ 800 成像仪在 SNOW 多重荧光模式下针对 Cy™3 和 Cy™5 染料拍摄。CyDye™ DIGE fluor Cy™3 和 Cy™5 预标记样本分别显示为绿色和红色。
2D 扩展分析
使用 IEF 分离后,将每条 Immobiline™ DryStrip 置于丙烯酰胺凝胶上,并进行 SDS-PAGE 分离。通过这种 2D 电泳方法,每个样本既通过使用 IEF 根据电荷变体进行分离,又使用 SDS-PAGE 根据分子量差异进行分离。进行了两组实验,分别使用 7 cm pH 3-10 NL(非线性)和 24 cm pH 3-10 L(线性)Immobiline™ DryStrip 凝胶。
所有 CyDye™ DIGE 预标记样本在 2D 电泳过程中均保持荧光标记。使用 ImageQuant™ 800 和 Amersham Typhoon™ 成像仪捕获 7 cm 和 24 cm Immobiline™ DryStrip 凝胶的荧光图像。图像数据通过 Melanie™ 9 在 3D 模式下可视化,并添加 pI 校准(图 4、5、6 和 7)。
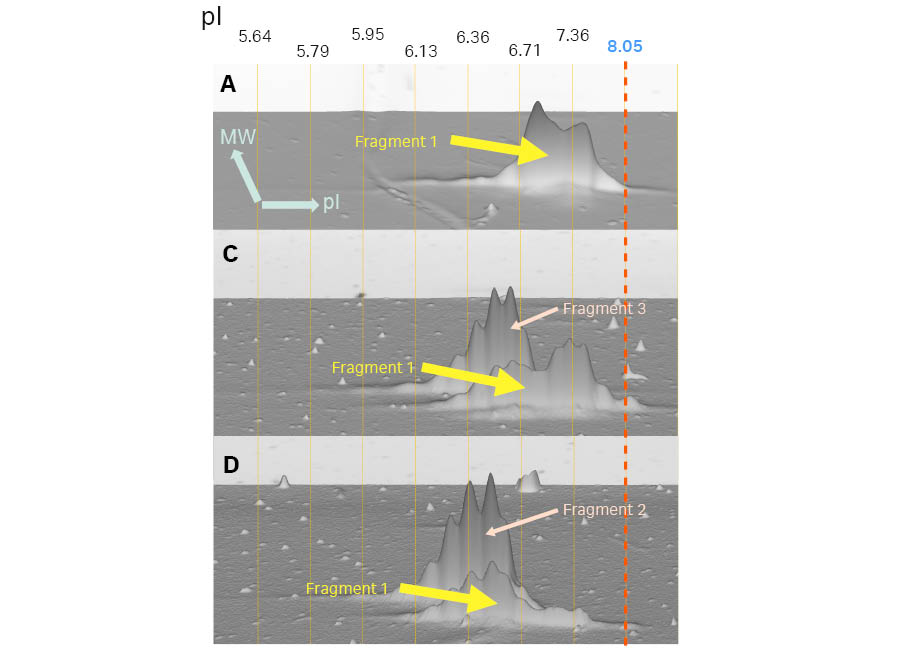
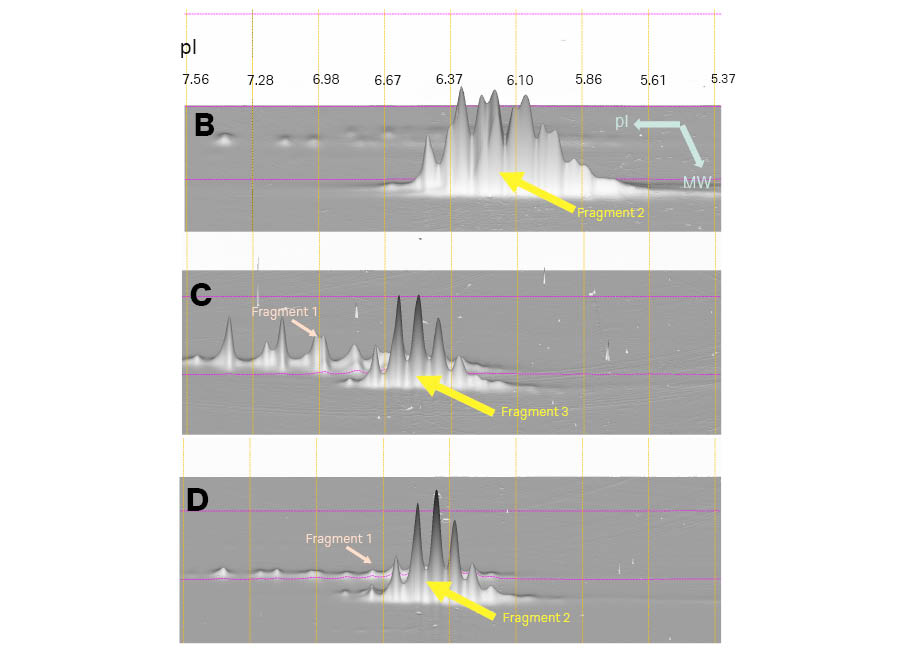
2D 扩展分析证实了样本 C 和 D 的 1D SDS-PAGE 结果,样本 C 和 D 各自含有具有不同表观分子量的片段(图 2)。使用带有 pI 校准的 3D 视图进行进一步分析,明确识别出每个片段的电荷变体。样本 A、C 和 D 中的片段 1,以同型二聚体(样本 A)表达时,相对于其与片段 3(样本 C)或片段 2(样本 D)形成异型二聚体时,表现出不同的电荷变体(图 5)。类似地,当片段 2 以同型二聚体(样本 B)表达时,或与片段 1 中形成异型二聚体(样本 D)时,也观察到电荷变化。片段 2 和 3 的差异在于,片段 3 中的 O-糖基化位点在片段 2 中通过电荷中和诱变被去除,从而导致不同的翻译后修饰。这种差异表现为电荷变体的差异,其中片段 2(样本 C 和 D)呈现轻微的酸性偏移(图 6)。
图 4.上部:样本 A、B、C 和 D 的 IEF 结果及对应的 2D 模式以 2D 视图显示,并带有 pI 校准。底部:2D 模式中每个片段的放大 3D 视图。虚线表示 2D 模式的 pI 校准。IEF 在 7 cm pH 3-10(非线性)Immobiline™ DryStrip 凝胶上进行。使用 ImageQuant™ 800 成像仪捕获图像,并使用 Melanie™ 9 软件进行分析。
图 5.样本 A、C 和 D 中片段 1(理论分子量为 39 000)的放大 3D 视图。此图中的 3D 视角是较低分子量侧。垂直线表示 2D 模式的 pI 校准。在样本 C 和 D 中,片段 1 位于较低分子量区域。
图 6.样本 B、C 和 D 中的片段 2(理论分子量为 47 000)和 3 的放大 3D 视图。此图中的 3D 视角是较高分子量侧。垂直线表示 2D 模式的 pI 校准。在样本 C 和 D 中,片段 2 位于较高分子量区域。
图 7 显示了 24 cm pH 3–10(线性)Immobiline™ DryStrip 凝胶的 2D 分析,其分辨率优于 7 cm pH 3–10(非线性)Immobiline™ DryStrip 凝胶。除分辨率外,两者在显示每个片段的电荷变体方面结果一致。
图 7.样本 B、C 和 D 中片段 2 和 3 的放大 3D 视图。此图中的 3D 视角为较高分子量侧。垂直线表示 2D 模式的 pI 校准。IEF 在 24 cm pH 3–10(线性)Immobiline™ DryStrip 凝胶上进行,并使用带有低荧光玻璃板的大尺寸凝胶(DIGE 凝胶)进行二维分析。图像使用 Amersham Typhoon™ 激光扫描仪扫描,并使用 Melanie™ 9 软件进行分析。
结论
我们已经展示了使用 DIGE 标记技术、等电聚焦电泳 (IEF) 和 Amersham ImageQuant™ 800 成像系统进行多重荧光检测,对修饰抗体片段(包括双特异性抗体)进行电荷变体分析,以支持生物制品开发。通过此方法,我们可以更好地从电荷和分子量变化两方面了解候选药物的分子特征概况。凭借 DIGE 多重方法,甚至可以检测到电荷和/或分子量变体的细微差异。这使得我们能够分析翻译后修饰(例如 O-糖基化)。
参考文献
(1) Beyer, B., Walch, N., Jungbauer, A., How Similar is Biosimilar? A Comparison of Infliximab Therapeutics in Regard to Charge Variant Profile and Antigen Binding Affinity. Biotechnology J.,2019;4. doi.org/10.1002/biot.201800340