高效保存、跟踪、监测和运输细胞制品的创新解决方案
细胞和基因疗法 (CGT) 正引领临床治疗变革,其治疗应用日益多元,全球范围内获批产品数量持续攀升。由于患者细胞是这些拯救生命疗法的基础,CGT 供应链在生物制品开发、制造和运输方面面临着前所未有的独特挑战。细胞需要特殊护理和考虑,例如严格的温度控制以及从采集到成品制剂的全流程追踪和验证能力。
目前用于应对这些挑战的许多工具和解决方案均依赖于实验室手工方法,此类方法耗时且存在相当大的风险。为确保充分释放 CGT 的潜力,我们必须升级解决方案,从而可靠地支持关键 CGT 原材料和产品的质控和运输。
CAR-T 细胞疗法的温度控制
CGT 是再生医学市场中增长极快的细分领域,迄今为止,大部分成功来自 CAR-T 细胞制剂。1,2这种免疫疗法适用于某些血液癌症,并在其他类型的癌症治疗中展现出潜力,其在无需额外治疗的情况下实现缓解的成功率约为 30% 至 40%。3 推动 CAR-T 疗法将对临床实践产生深远影响,尤其为已无其他治疗选择的终末期患者带来新生希望。随着 CAR-T 疗法在近年来获得美国 FDA 的一些重要批准,并具有改变预后的潜力,4这类药物的需求正在不断增长。为满足这一需求,CAR-T 生产商需要有效且高效的温度控制策略。
CAR-T疗法的起始材料采集始于临床,需由患者提供血液分离样本。随后,经过几个处理步骤制备样本以备运输,包括将提取的细胞在受控条件下冷冻至超低温(低于-120°C)。冷冻样本在运输至实验室或生产中心过程中,须全程维持超低温环境以防细胞活性衰减。处理完成后,成品制剂通常会再次冷冻保存以备运回患者。
冷冻保存是细胞制品温度控制的一种公认方法,但一直以来都需要专用空间、设备和培训才能正确执行。要处理冷冻保存材料,通常需要现场配备大型液氮罐、专用储存设施以及能在运输过程中容纳液氮而不会发生溢出或泄漏风险的运输容器。任何取回冷冻保存材料或运输大型运输容器的人员都必须接受液氮处理的专项培训。
为克服这些挑战并达到相关要求,CAR-T 细胞疗法开发商和制造商亟需专用设备,以在不使用液氮的情况下维持低温环境。Cytiva 推出的VIA Capsule™ 系统集成了运输单元、智能监测器和低温冷却器系统,使用电力将温度冷却至目标范围。该系统还可以跟踪和验证多个利益相关方之间的监管链(从采集到交付),为 CGT 原料生产质量保障再添关键一环。
管理 CGT 的监管链
自体 CGT 使用患者自身的细胞材料进行治疗。在整个复杂的工作流程中始终了解这些材料的位置对于确保质量、有效性以及交回给正确的患者至关重要。
起始材料可在医院或诊所采集,随后转交至处理实验室进行目标细胞分离和冷冻保存。制备完成的细胞制品随后被装入由诊所、快递公司或第三方提供的容器中进行运输。若 CGT 制造商与患者所在国家不同,则快递公司会将装有起始材料的容器运送至机场。抵达后,航空公司或地勤人员将材料搬运至飞机上,抵达目的地后交由另一家航空公司或地勤人员。随后,第二家快递公司将起始材料运送至制造工厂,将其转化为患者特异性治疗产品。处理完成后,这一复杂流程必须逆向操作,将治疗产品送回给患者。
目前,CGT监管链的管理方式是在产品转移过程中贴上带有唯一标识符的标签。同时采用纸质流程验证产品到达每个交接点的时间。该过程的透明度不仅对追踪至关重要,对确保时间线以防止批次丢失也至关重要。在传统生物制品生产中,产品丢失虽代价高昂,但仍可通过生产其他批次来满足患者需求。对于自体疗法,运输过程中任何错误或问题都可能对等待治疗的患者造成灾难性后果。因此,需要可靠的数字系统和软件解决方案,从起始材料离开诊所的那一刻起,直至最终治疗交付回给患者的时刻,进行全程追踪。
除提供无液氮运输选项外,VIA Capsule™ 系统还可与 CytivaChronicle™Chronicle™ 自动化软件。Chronicle™ 软件为细胞疗法机构提供统一的数字化平台,可实现生产运营与供应链物流的实时监控。这些创新工具可有效破解细胞疗法起始材料获取及相关供应链管理的极大行业难题。先进疗法治疗中心 (ATTC)、多家行业合作伙伴及公共部门的合作为这些解决方案的设计提供了支持。
ATTC 细胞疗法物流计划
2018 年,工业战略挑战基金拨款 3000 万英镑,支持在英国 (UK) 境内建立三家中心,即联合医院、先进疗法药物 (ATMP)制造商以及设备、软件和服务提供商,组成 ATTC网络。ATTC和其他专业中心旨在建立支持CGT临床供应、临床应用、数据采集及报销的系统。该网络可助力企业和 NHS 合作伙伴快速推进产品开发与市场准入,同时推动国际市场拓展。通过ATTC网络内的协调,英国国家医疗服务体系和行业组织可共同制定CGT产品交付的临床路径。
作为这些努力的一部分,ATTC 开展了一项研究,使用 Cytiva 的 VIA Capsule™ 系统和 Chronicle™ 软件开发和测试由制造商、快递公司、配送中心和临床试验中心组成的综合细胞疗法物流网络。简言之,SAMPLE(ATMP 组织收集标准方法)计划专注于获取 CGT 制造工作流程的起始材料,其愿景是:
- 减少 ATMP 变异性/失败(因样本质量标准不佳/不明确所致,且临床实践、设备和环境差异进一步加剧了此类问题)
- 通过明确采集调度流程并建立供应商与机构间的物流协作机制,简化交付并开发强大的互联供应链
- 确定 ATMP 起始物料采集的供应链薄弱环节(即关键设备、受培训人员、时间安排)
- 在采集点测试封闭式系统处理和冷冻保存,通过起始材料标准化实现 ATMP 工业化生产
本研究全程采用 Chronicle™ 软件,对漫长而复杂的 CGT 流程进行检查,并实现详细的数据采集与监测。首先,爱尔兰戈尔韦的科学家可扫描多个样本特定元素(包括运输工具),确认产品正确包装入 VIA Capsule™ 系统。随后,运输系统被送往英国伯明翰大学的 Orbsen™ Therapeutics 制造中心,在关键条件下使用 eSOPS 执行模拟卸载。运输数据再次被记录入 Chronicle™ 软件,实现全程监管链追踪,覆盖伦敦多个站点。当货物在物流链中从一个合作伙伴移动到另一个合作伙伴时,通过 Chronicle™ 平台内的远程监测功能实时跟踪位置和产品状况(图 1)。随后,细胞制品被送回 Orbsen Therapeutics,使用两种不同的活力检测方法进行最终评估。Orbsen 进行的测试明确表明,经过复杂运输过程并接受监测的样本细胞与储存在设施中的对照细胞在细胞活力方面无显著差异。5
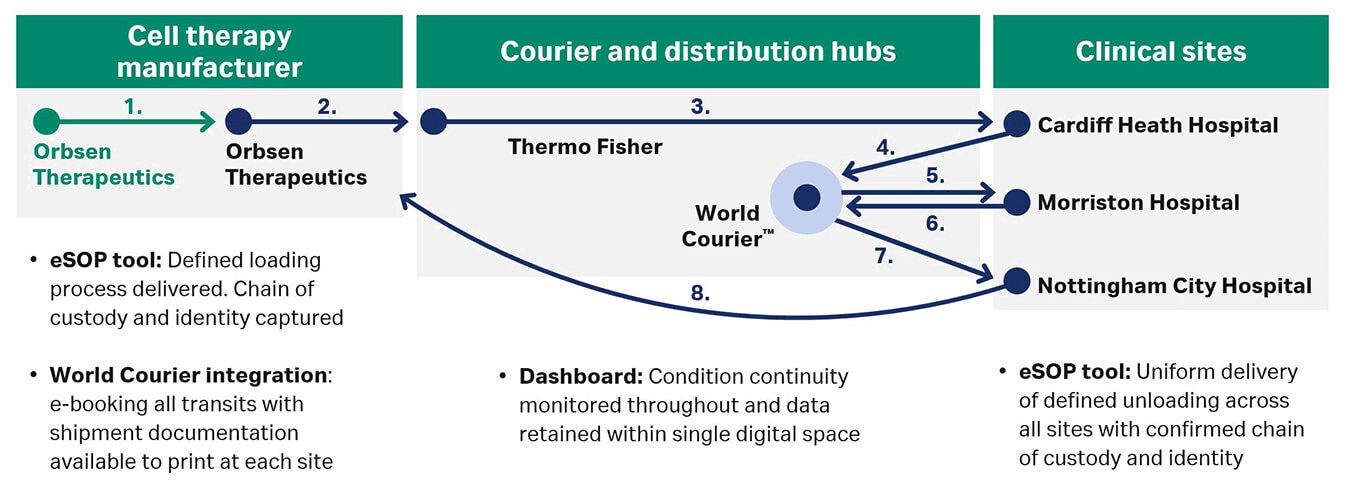
图 1.ATTC SAMPLE 研究的物流链。5
不断增长的 CGT 市场虽然充满机遇,但也面临诸多挑战。在行业探索新技术和新方法以提高生产效率、降低成本的同时,还必须确保关键原料从患者端到生产端再回输至患者端的全流程安全。自动化解决方案和协作努力(例如 ATTC 网络所展示的)是推动重要变革的关键要素,有助于实现 CGT 产品的规模化生产,从而满足患者与市场的需求。
参考文献
- Grand View Research. Gene Therapy Market Size, Share & Trends Analysis, Report Overview. Published Feb 2021. Accessed 22 March 2021.
- GlobeNewswire. The global cell and gene therapy market by revenue is expected to grow at a CAGR of over 30.90% during the period 2019–2025. Published 4 Aug 2020. Accessed 22 March 2021.
- Bartosch, J. UChicago Medicine. Three years after CAR T-cell therapy for lymphoma, patient still cancer-free. Published 17 October 2019. Accessed 22 March 2021.
- UPMC Hillman Cancer Center. FDA-approved CAR T-cell Therapies . Accessed 22 March 2021.
- Permission to publish ATTC SAMPLE study findings has been granted by Orbsen. Data available upon request.