亲和层析
什么是亲和层析?
亲和层析 (AC) 基于目的蛋白与附着在层析基架上的特异性配基之间的可逆相互作用来分离蛋白质。
这种相互作用可具有生物特异性,例如抗体结合蛋白 A 或受体结合激素;也可以是非生物特异性,例如蛋白质结合染料物质或含组氨酸的蛋白质结合金属离子,如螯合金属离子亲和层析 (IMAC)。
亲和层析如何工作?
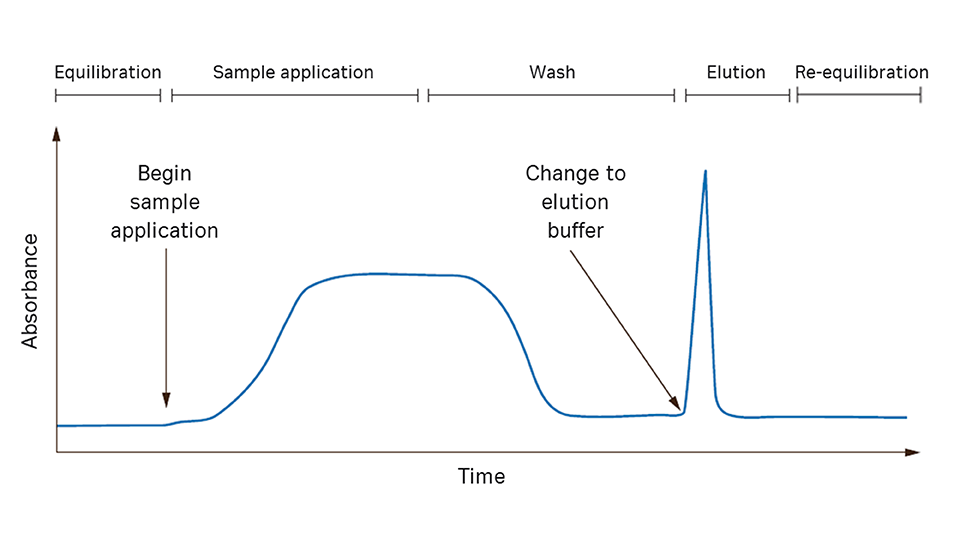
在亲和层析中,目的蛋白与互补结合物质(配基)发生特异性且可逆的结合。在有利于与配基特异性结合的条件下加载样本。未结合物质会被洗脱出层析柱。
通过将条件改变为有利于洗脱的条件,可回收结合的目的蛋白。可使用竞争性配基进行特异性洗脱,或通过改变 pH、离子强度或极性等参数进行非特异性洗脱。目的蛋白以纯化和浓缩的形式洗脱。
我应该何时使用亲和层析?
由于其高选择性,亲和层析可用于一步纯化。然而,更常见的是,AC作为第一步捕获步骤,随后进行一步或多步精纯步骤以去除残留杂质。
例如,与琼脂糖基架偶联的蛋白 A 或蛋白 G 配基可用于抗体的常规纯化。
如今,大多数实验室规模的纯化均采用亲和标签蛋白进行。带组氨酸标签的蛋白使用 IMAC 进行纯化,而谷胱甘肽 S-转移酶 (GST) 标签蛋白使用螯合谷胱甘肽的层析树脂进行纯化。
亲和层析也可用于去除特定杂质。