快速准确地检测病毒病原体对于治疗、监测、成功管理和控制流行病至关重要。核酸扩增检测 (NAAT) 是病毒检测领域的一种可靠、灵敏、准确的诊断方法 (1,2)。该方法涉及从样本中分离核酸,这不仅耗费时间和资源,还增加了意外污染和人为错误的可能性。
在需求高峰期(例如当前的 COVID-19 大流行期),核酸分离试剂盒的短缺会加剧依赖核酸的病毒检测方法的局限性。样本检测需求量大,使得诊断检测实验室难以及时提供准确结果。
直接逆转录聚合酶链反应 (RT-PCR) 技术可直接对未经纯化的样本进行检测,而无需分离核酸,有望减少样本检测所需的时间和资源。然而,要实现这一替代方案,必须克服样品中存在 RT-PCR 抑制剂导致的灵敏度下降以及核酸降解等技术瓶颈。Cytiva 开发了一种专有化学物质——抗抑制剂复合物 (AIC),有效解决了这些限制。在这一概念验证中,我们表明该化学技术可以实现无提取 NAAT,从而显著减少检测鼻咽拭子(保存于运输培养基中)病毒颗粒所需的时间和资源(图 1)。该专有配方提供了一种稳健的化学性质,其中样本中的低丰度核酸(例如病毒 RNA)稳定。该配方还通过增加 RT-PCR 酶对样本中抑制剂的耐受性来提高检测灵敏度。
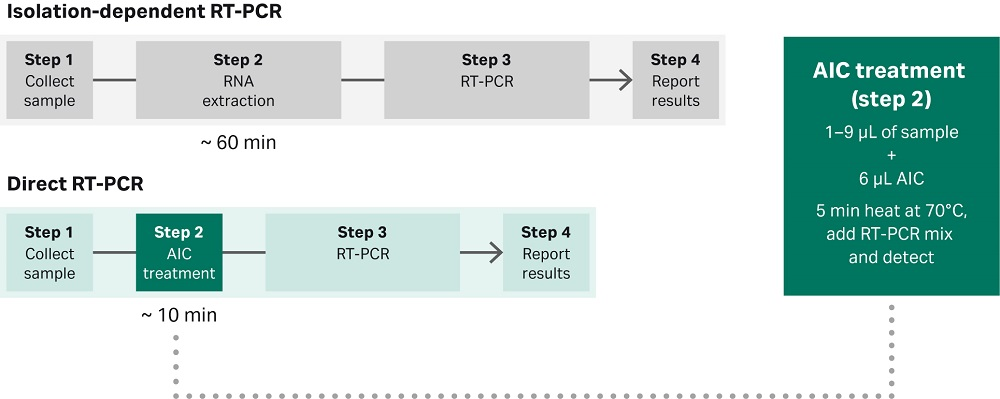
图 1.Cytiva RT-PCR 抗抑制剂复合物 (AIC) 可直接对未处理样本的核酸物质进行 RT-PCR 检测。专有的 RT-PCR AIC 无需核酸分离,仅需在 RT-PCR 反应前于 70°C 下进行短短五分钟的加热处理。
结果
通过将专有的 Cytiva AIC 配方与一步法逆转录和 DNA 扩增 (RT-PCR) 试剂盒相结合,我们提高了检测未纯化样本中病毒颗粒的灵敏度、可重复性和稳健性。如图 2:A-B 所示,Cytiva 的 AIC 化学技术可直接从未纯化鼻咽样本中检测病毒 RNA,每次反应中加标少至 10 拷贝,无需核酸分离,从而降低了成本并缩短获得结果的时间。
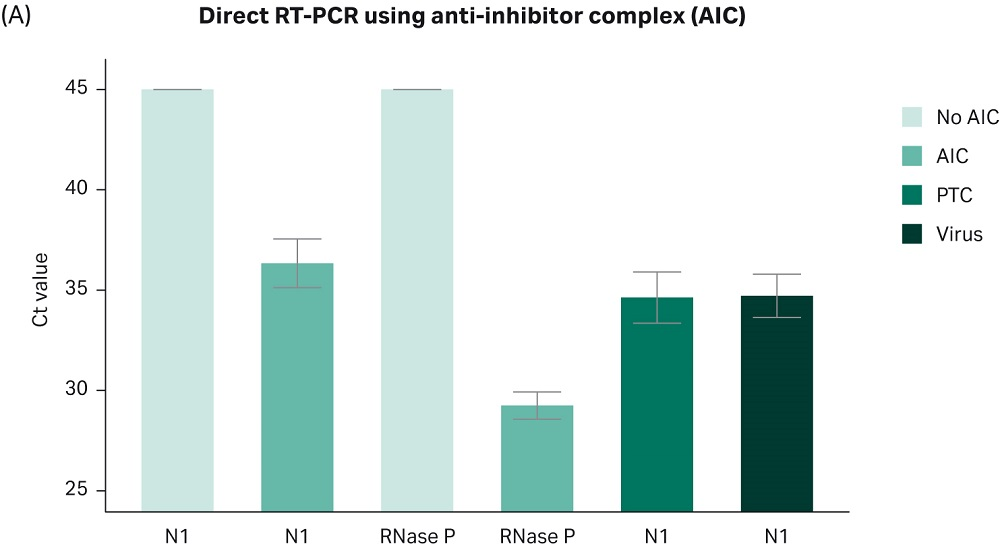
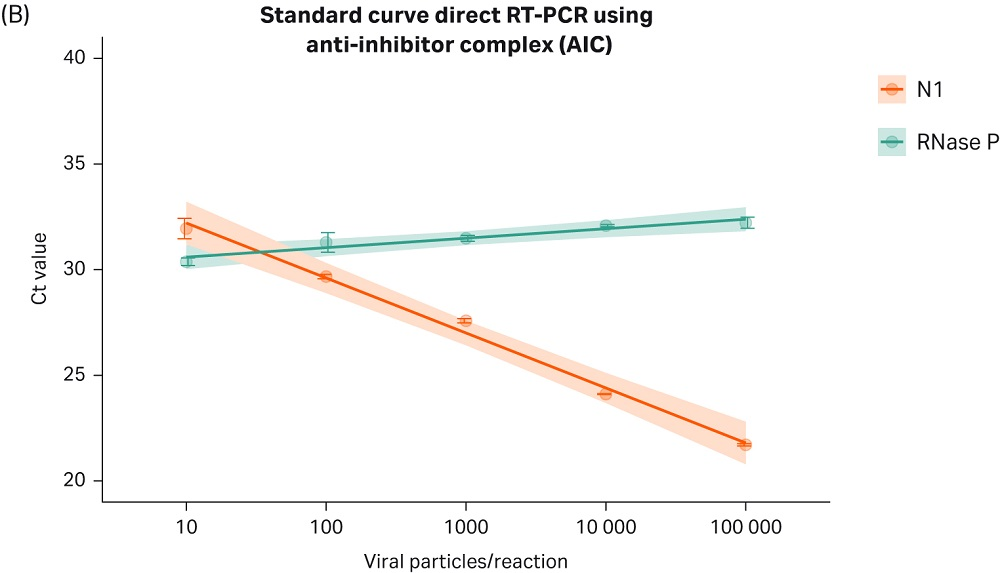
图 2.Cytiva RT-PCR AIC 混合液可直接对未纯化的患者样本中的 COVID-19 病毒颗粒进行稳健、灵敏和准确的检测。实验采用保存于运输培养基中的人鼻咽拭子(COVID-19 阴性患者样本,Tissue Solutions,FM 参考号:QQPE7),并添加不同浓度的热灭活 SARS-CoV-2 病毒颗粒(SeraCare™,货号 0505-0126、批号 10481654;或 ATCC VR-1986HK)。取 5 µL 样本与 6 µL AIC 试剂混合,于 70°C 下加热 5 分钟,加入引物(IDT Primes、N1 或 RNase P、2019-nCoV RUO 试剂盒:Integrated DNA Technologies™、货号 10006713) 和 RT-PCR 主混液。逆转录和扩增反应采用一步法,遵循试剂盒制造商的建议(TaqPath™ 1-step Multiplex Master Mix 进行 RT-PCR,Applied Biosytems™,货号 A28525)。(A) 柱状图显示使用针对 SARS-CoV-2 病毒 N 基因的引物组 N1 通过实时 RT-PCR 获得的 Ct 值。该图显示了三次独立实验的合并结果 ± SD,每次运行三次技术重复。使用阳性对照引物,其靶向作用于人 RNase P 基因,可扩增人细胞的基因组物质。质粒模板对照 (PTC)(20 cp/反应):编码病毒颗粒中所含相同人工序列的质粒。病毒(10 cp/反应):含有部分 SARS-CoV-2 病毒基因组的人工病毒。(B) 实时 RT-PCR 标准曲线显示了在广泛病毒载量范围内对病毒 RNA 的线性和灵敏检测。实验按上述方法进行。每次反应的病毒载量范围为 10-10e5 个颗粒。
COVID-19 NAAT 检测时,鼻咽拭子是从患者身上采集的推荐样本类型。这些拭子通常储存在运输培养基中,而运输培养基本身可能抑制扩增反应。尽管如此,目前市售 RT-PCR 试剂盒对运输培养基的耐受性有限。这种耐受性最高仅达反应体积的 25% (3,4),并可能限制检测性能,尤其是在处理低病毒载量样本时,例如在某些 COVID-19 患者的样本中,其病毒载量随疾病进展而变化 (5,6)。因此,更广泛的运输培养基耐受性可能有利于成功检测低病毒载量。解决这一限制的一种方法是将优化的一步法 RT-PCR 主混液配方与 RT-PCR 抗抑制剂复合物相结合。这就是 Cytiva 的直接 RT-PCR 化学技术,该技术对运输培养基表现出高耐受性,即使样本运输培养基体积达到最终反应体积的 45% 也能够检测到低病毒载量(图 3)。这在检测临界阴性/阳性样本时具有优势,可通过将检测样本体积翻倍而不影响检测灵敏度。
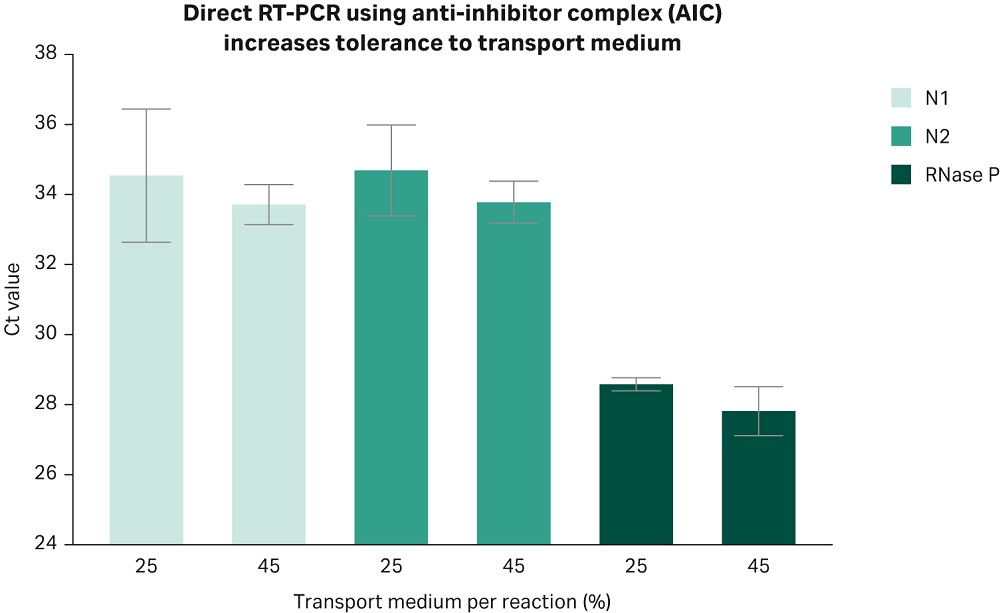
图 3.Cytiva 直接 RT-PCR 化学技术可耐受大体积运输培养基,因而允许使用更大体积的患者样本。柱状图显示使用针对 SARS-CoV-2 病毒 N 基因的引物组 N1 和 N2 通过实时 PCR 获得的 Ct 值。该图显示两项独立实验,每个实验运行三次技术重复。靶向作用于人 RNase P 基因的引物(可扩增人细胞的基因组物质)用作阳性对照。(N1、N2 和 RNase P 引物,2019-nCoV RUO 试剂盒:Integrated DNA Technologies,货号 10006713). 实验采用 COVID-19 阴性捐赠者的鼻咽样本,添加浓度为 2.5 cp/µL 的热灭活 SARS-CoV-2 病毒颗粒(SeraCare,货号 0505-0126、批号 10481654;或 ATCC VR-1986HK)。将 5 µL (25%) 或 9 µL (45%) 的该溶液与 6 µL AIC 混合液混合,于 70°C 下加热 5 分钟,然后加入 RT-PCR 主混液(Cytiva 一步法 RT-PCR 混合液)。
在当前 COVID-19 疫情期间,公共卫生组织和诊断实验室面临的挑战之一是用于样本采集的运输培养基短缺。这导致用于 NAAT 的 COVID-19 样本采集出现不一致。美国疾病控制和预防中心 (CDC) 建议使用可在当地制备的替代采集培养基,包括 PBS、盐水 (0.9% NaCl) 或更广泛使用的标准通用病毒运输培养基(适用于细胞培养)(7,8)。我们测试了直接 RT-PCR 化学技术在不同运输培养基中采集的患者样本病毒颗粒检测性能。图 4 显示,Cytiva 的直接 RT-PCR 化学技术可在广泛的动态范围内检测病毒载量,无论使用何种运输培养基。
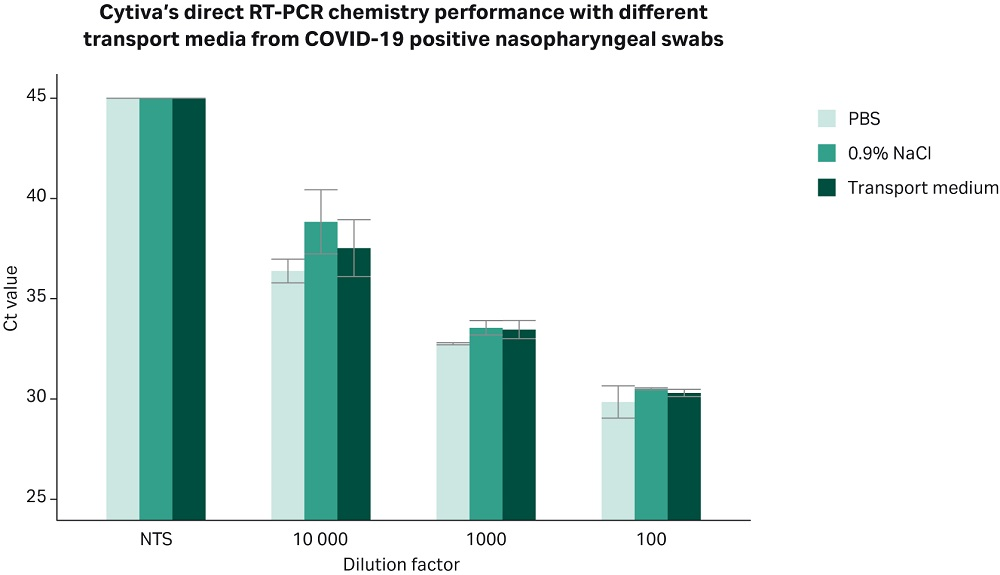
图 4.Cytiva 的直接 RT-PCR 化学技术可直接从多种运输培养基保存的未纯化鼻咽样本中稳健、灵敏地扩增病毒核酸。柱状图显示使用针对 SARS-CoV-2 病毒 N 基因的引物组 N1 通过实时 PCR 获得的 Ct 值。简而言之,在 COVID-19 阴性鼻咽拭子样本池中加入先前由奥地利开普勒大学附属医院临床检测中心确认为 COVID-19 阳性的鼻咽拭子样本梯度稀释液。样本分别保存于 PBS、生理盐水或商业运输培养基系统中。本实验中使用的运输培养基系统根据 CDC 在参考文献 (7) 中描述的指南制备。所有样本均按先前实验描述的方法处理。简言之,将 5 µL 样本与 6 µL AIC 试剂混合,于 70 °C 下加热 5 分钟,然后加入引物(N1 引物、2019-nCoV RUO 试剂盒:Integrated DNA Technologies,货号 10006713) 和 Cytiva AIC 混合液。由于患者样本获取受限,该图显示的是单次实验的三重复结果。误差线表示测量值的标准差。X 轴显示了实验中使用的梯度稀释液的 -log10 值。
将无提取化学技术应用于未纯化样本的病原体检测,是一项超越 COVID-19 检测的挑战。在原理验证实验中,我们在来自“健康”捐赠者的鼻咽样本中添加了合成 rEbola 病毒颗粒(AccuPlex rEbola 参比品,SeraCare,货号 0505-0001,25 cp/µL 样本)。尽管此设置并不代表埃博拉病毒检测的真正模型,但结果表明,在鼻咽样本的复杂条件下,Cytiva 的直接 RT-PCR 化学技术可对 rEbola 病毒颗粒进行一致、可靠的检测(图 5)。目前正在进行进一步研究以验证这些结果,并扩大该技术在临床和宏基因组学应用中的样本类型范围。这为有意开发本研究未重点介绍的其他病原体和样本类型的无提取 NAAT 的检测开发人员提供了机遇。
图 5.Cytiva 的直接 RT-PCR 化学技术可检测埃博拉合成病毒颗粒。实验采用保存于运输培养基中的人鼻咽拭子(COVID-19 阴性患者的鼻咽拭子,Tissue Solutions,FM 参考:QQPE7),并添加 25 cp/µL 热灭活 rEbola 病毒颗粒(SeraCare,AccuPlex™ rEbola GP/NP 参比品,货号 0505-0001)。取 5 µL 样本与 6 µL Cytiva AIC 试剂混合,于 70°C 加热 5 分钟,然后加入引物(GP 基因:基于水解探针的检测引物根据参考文献 (9) 设计,IDT 引物:RNase P,2019-nCoV RUO 试剂盒:Integrated DNA Technologies,货号 10006713) 和 RT-PCR 主混液。逆转录和扩增反应按照试剂盒制造商的建议一步完成(Cytiva 一步法 RT-PCR 混合液)。柱状图显示了使用针对扎伊尔埃博拉病毒 GP 基因的引物组 GP 通过实时 PCR 获得的 Ct 值。该图显示了两次独立实验的合并结果 ± SD,每次运行三次技术重复。靶向作用于人 RNase P 基因的引物(可扩增人细胞的基因组物质)用作阳性对照。
结论
Cytiva 的直接 RT-PCR 化学技术由专有 AIC 和 RT-PCR 主混液组成,实现了免提取的核酸扩增检测 (NAAT)。这是一种快速、准确、灵敏的检测方法,可直接从未纯化的鼻咽患者样本中检出病毒 RNA,从而降低检测成本并。更重要的是,检测结果的出具时间得以缩短。此外,该化学技术用途广泛且稳定:可提高样本中 RNA 的稳定性,增强对病毒运输培养基的耐受性,并扩大可直接从未纯化样本中检测的病毒核酸靶标和病原体的范围。使用 Cytiva 的直接 RT-PCR 化学技术,我们能够检测到每次反应低至约 10 个拷贝的 SARS-CoV-2 病毒颗粒。我们正在进行进一步的研究,以评估不同的样本类型和病原体。
直接 RT-PCR 化学技术为受核酸分离试剂盒和耗材短缺造成的瓶颈影响的核酸检测 (NAT) 方案提供了一种便捷的替代方案。该方法有助于检测实验室优化 NAT 工作流程、加速高通量检测,并降低交叉污染风险及相关设备成本。迄今为止,遗传性疾病和传染病的诊断仍需要昂贵且耗时的程序。我们相信,该化学技术作为筛查诊断工具,可缩短患者确诊周期,仅对初始检测阴性但高度疑似感染的样本进行 RNA 提取试剂盒复检。
有关 Cytiva 的直接 RT-PCR 化学技术的更多信息,请联系我们的定制服务团队,提交询问,或咨询您的产品专员。
Cytiva 直接 RT-qPCR 试剂盒目前仅可供研究使用 (RUO)。
参考文献
- Zhang et al. Journal of Medical Virology, 2020: Recent advances in the detection of respiratory virus infection in humans.
- Tahamtan & ARdebili. Expert Review of Molecular Diagnostics, 2020: Real-time RT-PCR in COVID-19 detection: issues affecting the results.
- https://international.neb.com/-/media/nebus/files/application-notes/sars_cov2_detection_an.pdf?rev=6c002a18330747de8a1553bd78f1ea17
- https://www.takarabio.com/products/covid-19-research/viral-detection-with-qpcr/direct-viral-detection-via-qpcr
- He et al. Nature Medicine, 2020. Temporal dynamics in viral shedding and transmissibility of COVID-19.
- Holshue et al. New England Journal of Medicine, 2020. First Case of 2019 Novel Coronavirus in the United States.
- https://www.cdc.gov/coronavirus/2019-ncov/downloads/Viral-Transport-Medium.pdf
- https://www.cdc.gov/coronavirus/2019-ncov/lab/faqs.html
- Pinsky et al. PLOS One, 2015. Analytical Performance Characteristics of the Cepheid GeneXpert Ebola Assay for the Detection of Ebola Virus.