血液成分分离术在细胞免疫疗法开发中的应用
最近的科学进展加深了人们对癌症的认识,并推动了个性化药物(如免疫疗法)的开发。
基于 T 细胞受体 (TCR) 的治疗方法,例如 CAR-T 细胞疗法,已成为研究重点,并最终可能在癌症治疗标准中发挥重要作用。迄今为止,FDA 仅批准 CAR-T 细胞疗法在临床用于特定类型的白血病和淋巴瘤,且限于经认证的癌症中心。然而,Kymriah™ (Novartis) 和 Yescarta™ (Gilead/Kite) 免疫疗法的成功,为开发类似的新型有效策略以潜在消除耐药性肿瘤奠定了基础。
细胞疗法利用自体或异体基因修饰细胞进行开发。由于源产品材料固有的显著变异性,使这些治疗方法(及其制备流程)适应不同患者,仍然是标准化免疫疗法面临的关键挑战。
单采外周血采集技术因其微创且能收集大量细胞,成为了获取细胞疗法患者源材料的首选方法。任何通过单采收集的生物制品,若存在变异性增加或质量下降的情况,均可能对后续处理产生负面影响,因此这一步骤对治疗本身的成功至关重要。细胞疗法制造商可能需要采用子流程、决策矩阵及更复杂的分析方法来应对产品原料变异性。此外,一旦转入商业化阶段,患者数量和采集点数量均会增加,对供应链和起始材料的稳健性要求也随之提升。
本文汇集了关于单采产品及其特性、采集方式和处理的资源和信息。本报告旨在为细胞疗法的单采采集及富集产品获取提供指导和最佳规范。
血液成分分离术的工作原理
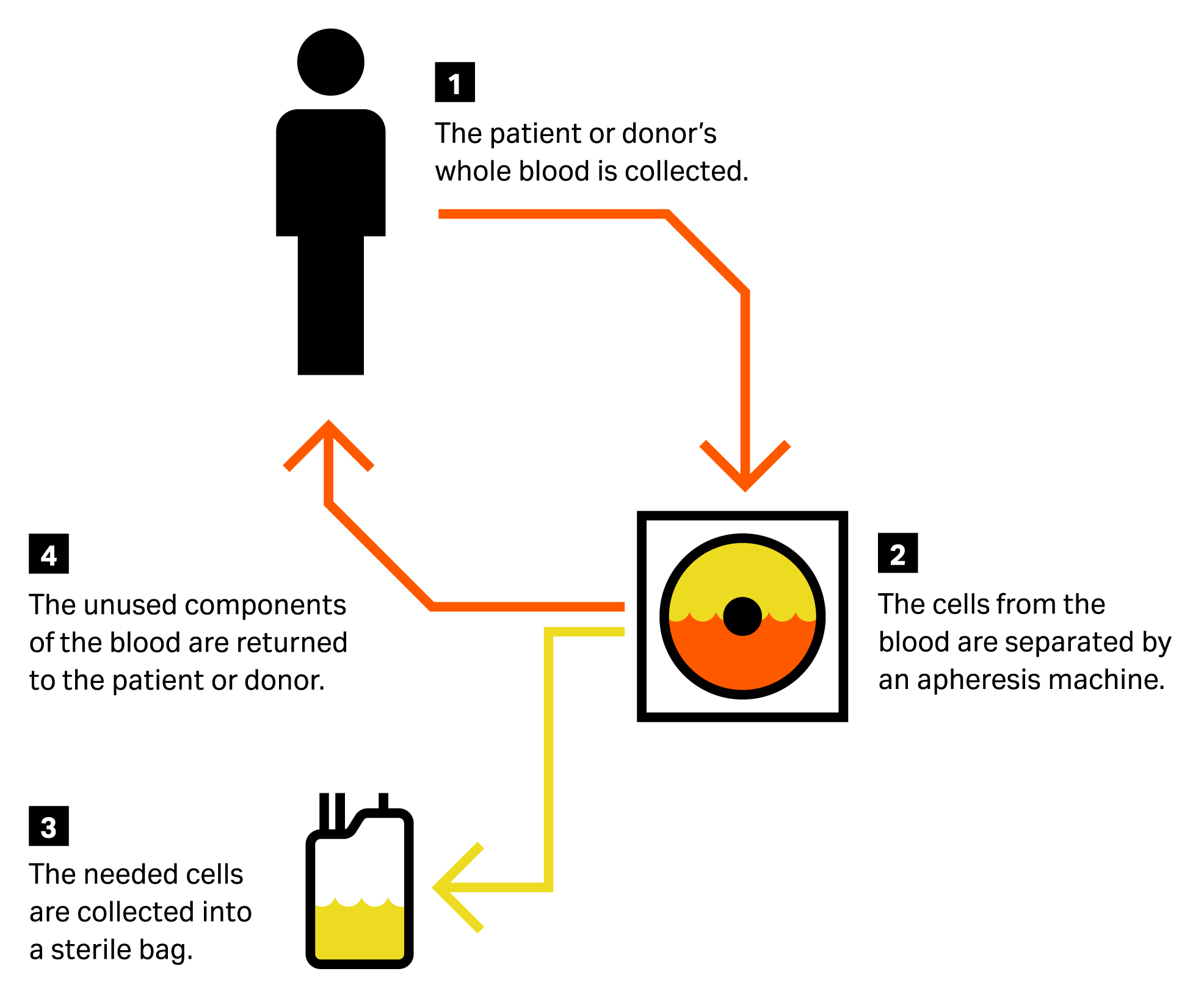
血液成分分离是指对患者进行的一系列操作,用于去除外周血并分离外周血成分。血液成分分离采集设备用于收集并分离某些成分(例如血浆、血小板和白细胞),然后将剩余部分重新输入患者体内(图 1)。不同类型的血液成分分离包括红细胞单采术(保留红细胞)、白细胞单采术(保留白细胞)、血浆单采术(保留血浆)和血小板单采术(保留血小板)。
再生医学和细胞处理的输血中心使用白细胞分离术分离白细胞(淋巴细胞、单核细胞、干细胞等),这些白细胞可用于体外生物工程化患者特异性细胞疗法(自体治疗)。
图 1.血液成分分离过程图解。
我们通常将白细胞分离术分为两种类型:动员型和非动员型。
动员型血液成分分离术的目标是获取造血干细胞 (HSC)。在动员型血液成分分离术中,患者/捐献者需要在血液成分分离术采集前进行预处理,以将 HSC 从骨髓转移到外周血。
在非动员型血液成分分离术中,患者/捐献者无需接受预处理。此类血液成分分离术的目标是获取分化细胞,例如 B 和 T 淋巴细胞或单核细胞。这种患者特异性源产品为免疫疗法的开发提供了起始材料。
血液成分分离术中的多种变异来源
尽管源产品存在差异,但开发一种灵活且适合所有患者的工艺仍是免疫疗法制造中的一大挑战。与血液成分分离术相关的诸多变量必须予以考虑,包括:
- 患者特定变量,例如年龄、民族和诊断
- 所用血液成分采集设备的性能
- 运输和储存条件,例如缓冲液和温度
- 单采血液产品处理后的血液成分变异性
其中部分变量可实现标准化,而另一些患者特异性变量可能无法控制。以下工艺控制策略可最大限度地减少患者固有变异性、提供更可预测的细胞疗法产品、并实现更一致的治疗安全性和有效性特征,从而实现最佳患者治疗。
实现血液成分分离术标准化,以减少差异
许多参数会影响用于制造细胞疗法的材料质量并影响最终产品。这些参数包括独特的捐献者特征、血液成分采集设备以及运输和储存条件。1,2 在可控范围内,保持这些因素的一致性有助于减少工艺和产品变异性。
运输和储存条件
经过血液成分采集处理后,细胞制品材料必须储存并从中央处理中心运出。确定细胞疗法在不同地点之间储存和运输的最佳条件是维持高细胞活力的关键。过去几年中,已发表了大量涉及健康志愿者的研究,这些志愿者通过血液成分分离术收集非动员型单核细胞 (MNC),以确定最佳储存条件。3
这些研究揭示了以下内容:
- 冷藏储存(4°C 至 8°C)比室温 (RT) 储存(20°C 至 22°C)更能保持细胞活力,尤其是对于细胞浓度较高的产品。
- 高细胞浓度下室温保存会导致白细胞相对减少。
- 在许多血液成分分离程序中观察到血小板活化,诱导单核细胞与血小板聚集。
总之,建议在所有程序中使用相同的采集设备,并在 4°C 下储存和运输血液成分分离制品,以最好地保存和维持细胞活力、细胞数量和表型。
提高高度可变血液成分分离参数的可管理性
细胞含量异质性和 MNC 富集
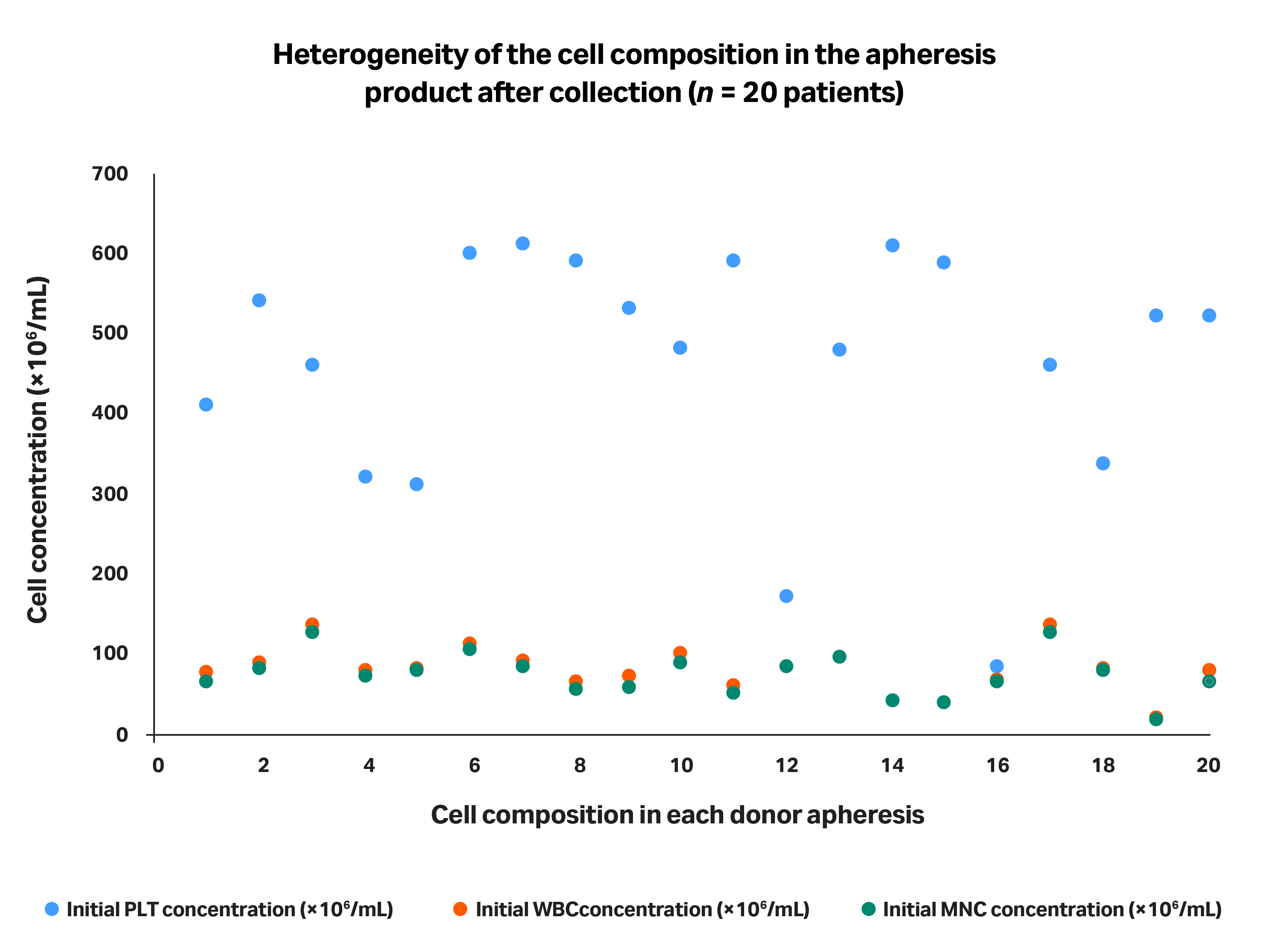
图 2 突出显示了使用相同采集装置处理几种血液成分分离制品后细胞组成的异质性。
图 2.使用相同采集设备处理后,血液成分分离制品在细胞组成方面的异质性示意图。每列数据代表 20 例患者的汇总结果。
为了血液成分分离术后血液中获取单核细胞层,需进行第二个细胞处理步骤以去除血小板、红细胞 (RBC) 和粒细胞,从而富集 MNC。该步骤的目标是减少由这些细胞群引起的异质性,并最大限度地减少患者间差异导致的组成差异。同时,此步骤可最大限度地获得所需单核细胞群的收率。以更高的起始细胞数量开始离体制造工艺可增强细胞表型分离过程中的稳健性,并加快细胞扩增步骤所需的时间,使您能够更快地获得所需的最终剂量。
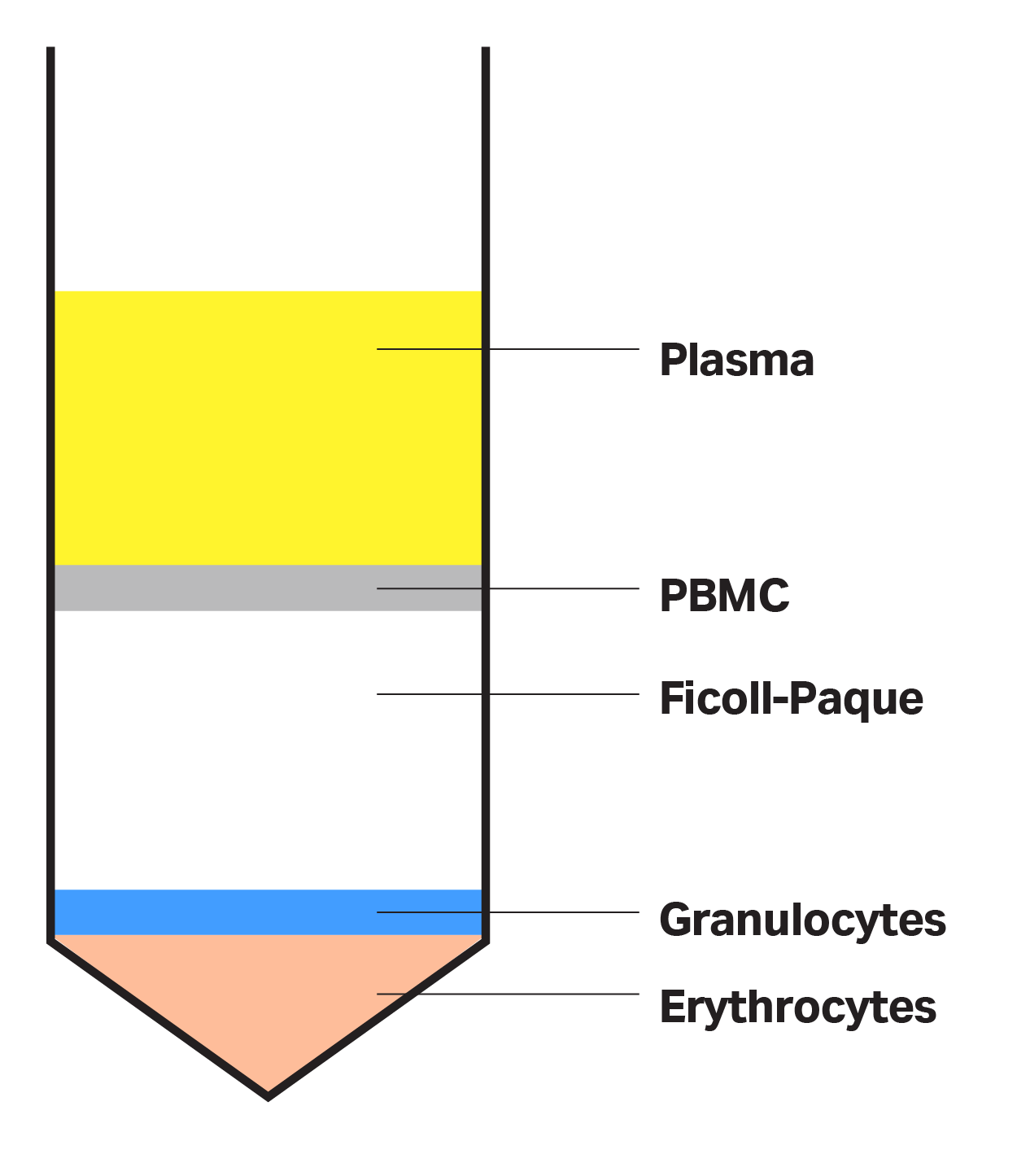
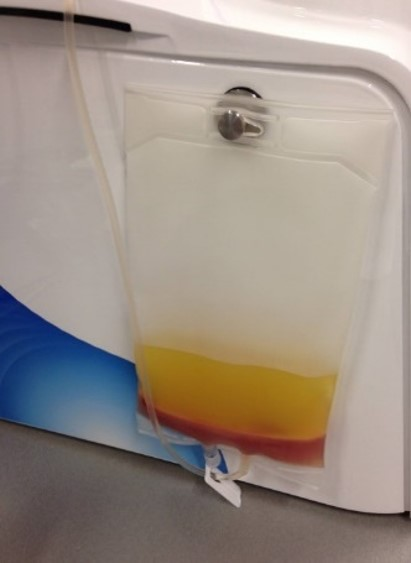
在此富集阶段,单个核细胞(例如单核细胞和淋巴细胞)根据不同的组分密度,与血小板、血浆、红细胞和粒细胞 (GRC) 分离。您可使用密度梯度分离培养基(例如 Cytiva 的 Ficoll-Paque™ 培养基)实现这种分离。Ficoll™ 培养基具有特定的密度 (1.077 g/mL),介于红细胞和粒细胞的一侧密度与单个核细胞、血小板和血浆的另一侧密度之间。密度梯度培养基层可有效分离离心后的不同组分,底部为高密度细胞(例如红细胞),顶部为含有血浆和血小板的低密度层(图 3)。
图 3.Ficoll-Paque™ 密度梯度分离培养基将低密度血液成分与高密度红细胞和粒细胞分离。
去除不会用于治疗的细胞可减少变异性并提高标准化程度。此外,这些不需要的细胞若被纳入免疫治疗制剂中,可能导致不良结果。
去除红细胞非常重要,因为红细胞污染会使最终细胞疗法呈现红色——药品监管机构可能将其视为杂质,导致产品不符合标准。早期阶段去除血浆和血小板,也可抑制血小板活化,帮助成功清除其他不需要的细胞。活化的血小板可能附着于其他细胞并形成聚集或团块,从而改变细胞密度并影响密度梯度培养基分离的效率。已知可诱导血小板活化的其他因素包括:高细胞浓度、长时间储存、缺乏钙螯合剂、所用采集装置类型以及离心过程中产生的强机械力。
案例研究:确定 MNC 富集的出色方案
我们研究了最大限度减少初始血液分离术获得的 MNC 富集产品变异性的最佳实践,旨在实现患者间流程标准化,从而提高免疫疗法生产过程的可控性和可预测性。
历史上,MNC 富集过程的前几步包括:
- 输入产品的浓缩
- 通过密度梯度培养基去除红细胞
该过程有时会导致以下问题:
- 血小板附着于单核细胞(聚集形成)
- 单核细胞活力下降
- 红细胞污染(通过评估最终产品的颜色判断)
通过将红细胞污染程度(红色)与初始血液成分分离样本的特性(细胞成分重新分布)相关联,提出了以下假设:
- 红细胞污染可能与输入血液成分分离制品的血小板含量相关
- 在红细胞分离前去除血小板有助于避免血小板活化,从而避免血小板聚集和影响红细胞分离的效率
基于此经验,我们认为血小板计数在富集过程的初期阶段发挥着重要作用。血小板计数高会影响红细胞分离。因此,我们建议流程。因此,我们建议流程时降低并标准化血小板计数。
为支持这一建议,我们进行了一项额外的研究,以评估在红细胞分离前降低血小板计数 的获益,该研究比较了:
i. 去除血小板后分离红细胞的 MNC 富集效率
中间产品袋
终产品袋
ii. 直接对高血小板浓度的产品进行红细胞分离的 MNC 富集效率
中间产品袋
终产品袋
早期去除血小板有助于减少密度梯度分离过程中的红细胞污染。尤其是初始产品含有大量血小板时,效果更显著。
其他注意事项:
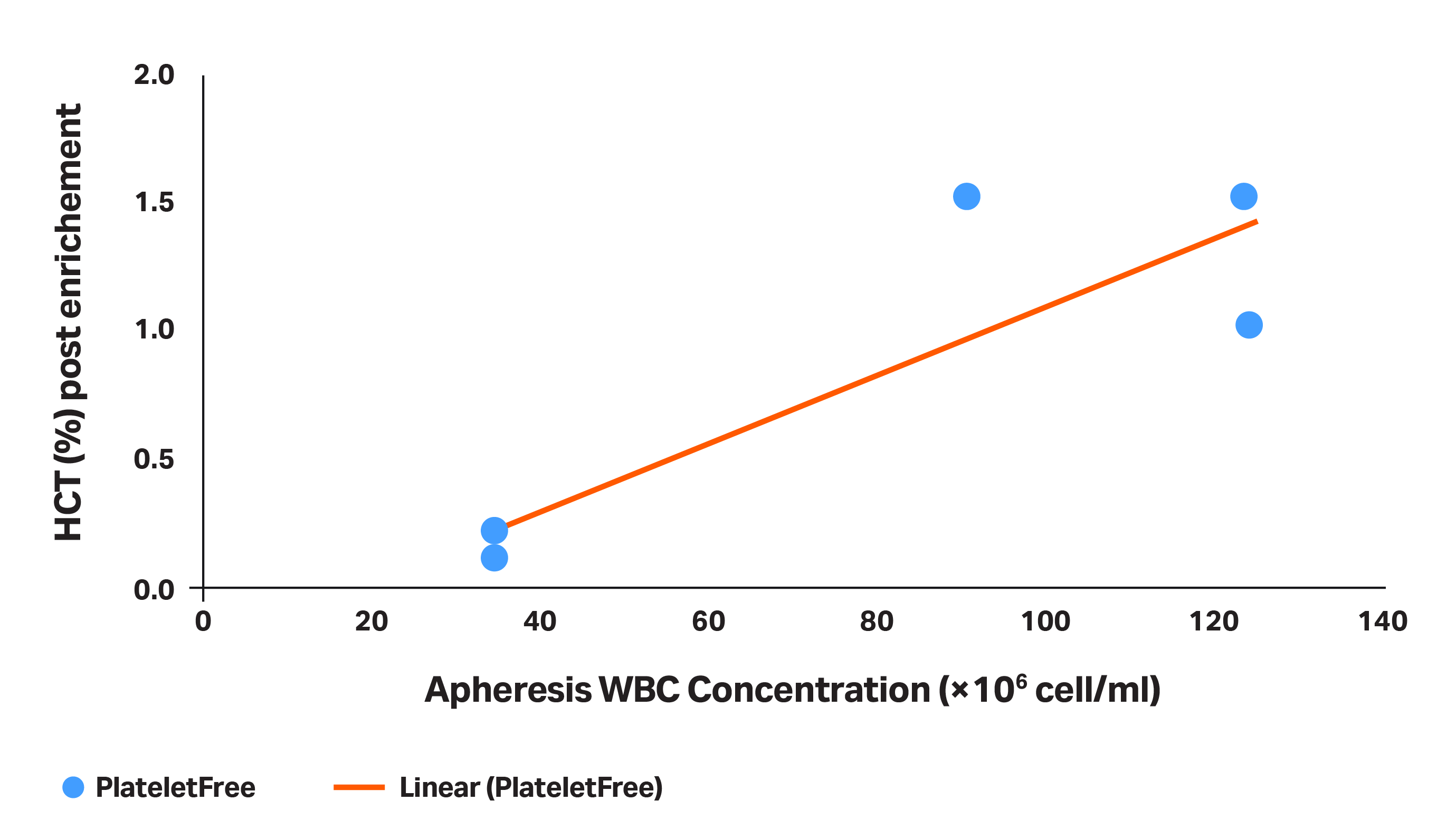
- • 血液成分分离术的白细胞浓度会影响红细胞分离的有效性。除了血小板计数外,初始血液成分分离制品中的白细胞浓度也会影响红细胞分离的成功率。随着白细胞浓度增加,红细胞污染的风险也随之升高。对于初始白细胞浓度高于 80 至 100 × 106个细胞/mL 的血液成分分离样本,您不太可能使 MNC 富集产品的血细胞压积明显低于 1%(图 4)。
图 4.MNC 富集(血小板去除 + 红细胞分离)后产品中获得的 HCT (%),作为白细胞浓度的函数。
- 不同采集中心提供的血液成分分离制品可能具有不同特性。根据我们的直接经验,血液成分分离术提供商拥有不同规模的捐献者群体,且采集产品的频率各不相同。一般而言,采集频率越高,捐献者材料中活化血小板数量就越多。4
注意:一些客户报告,更换采集中心时出现与 Ficoll™ 分离相关的问题。
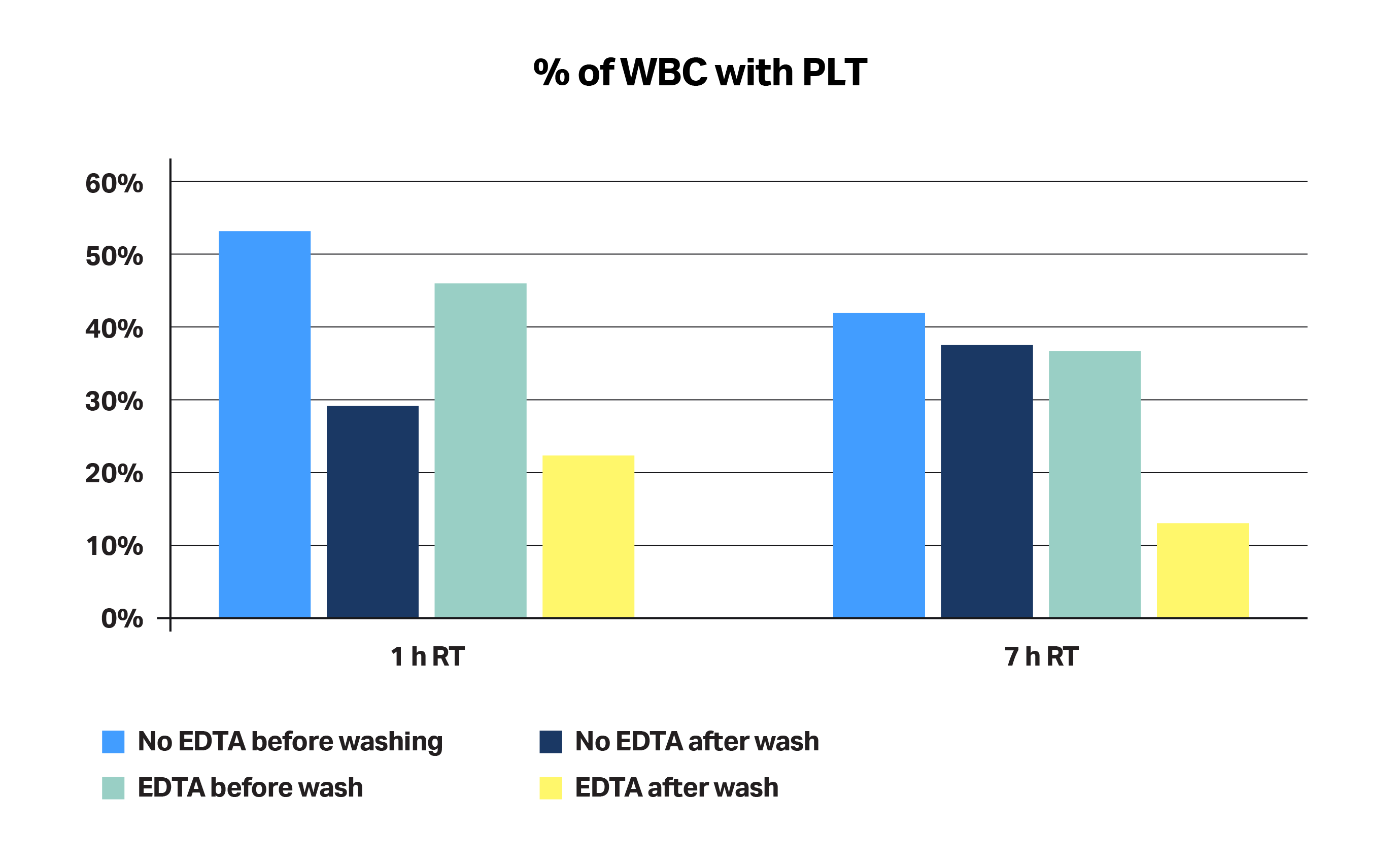
所用缓冲液的类型可最大限度地降低细胞聚集体形成的风险。在血液成分分离制品运输和洗涤过程中,使用含钙螯合剂的缓冲液(例如 EDTA)可最大限度地减少附着白细胞上的血小板百分比,从而降低细胞聚集体对红细胞分离产生负面影响的风险(图 5)。血液成分分离制品采集自健康捐献者,并在室温下于 24 小时内运送。采用流式细胞术进行分析,观察血小板活化标志物(P-选择素/CD62-P)。我们发现,若不使用 EDTA(钙螯合剂),血小板无法被有效洗脱。
图 5.附着于血小板的白细胞百分比。通过流式细胞术进行分析,观察血小板活化标志物(P-选择素/CD62P)。
标准化 MNC 富集的附加建议
为了进一步降低初始血液成分分离制品的变异性,请考虑以下策略:
- 采集后立即用添加 1 mM EDTA(或其他钙螯合剂)的溶液稀释血液成分分离制品,以避免血小板活化和聚集。该溶液必须基于磷酸盐缓冲盐水(PBS,不含 Ca++ 和 mg++)或标准生理盐水。也可添加白蛋白或血清,以进一步增强稳健性和细胞保护。
- • 处理材料时,最大密度不超过约106个细胞/mL,以最大限度地减少细胞聚集。在整个富集过程中,在冷藏温度下运输和储存产品。
表 1.非标准化 (A) 流程与标准化 (B) 流程的详细信息
|
收集 |
运输 |
PLT 去除 |
RBC 去除 |
|
|
非标准化流程 (A) |
未系统性地使用相同的采集设备 采集频率约为每 6 至 8 周一次 处理后未控制细胞密度 |
处理后未控制细胞密度 使用基础缓冲液进行细胞稀释/洗涤 |
无 | 有 - 第一步(和最后一步) |
|
标准化流程 (B) |
使用相同的采集设备 采集频率约为每 10 至 12 周一次 处理后最大密度不超过106/mL |
温度控制在 4°C 使用含钙螯合剂的缓冲液 (EDTA) |
有 - 第一步,针对去除 PLT 优化离心力/沉降条件 | 有 - 第二步 |
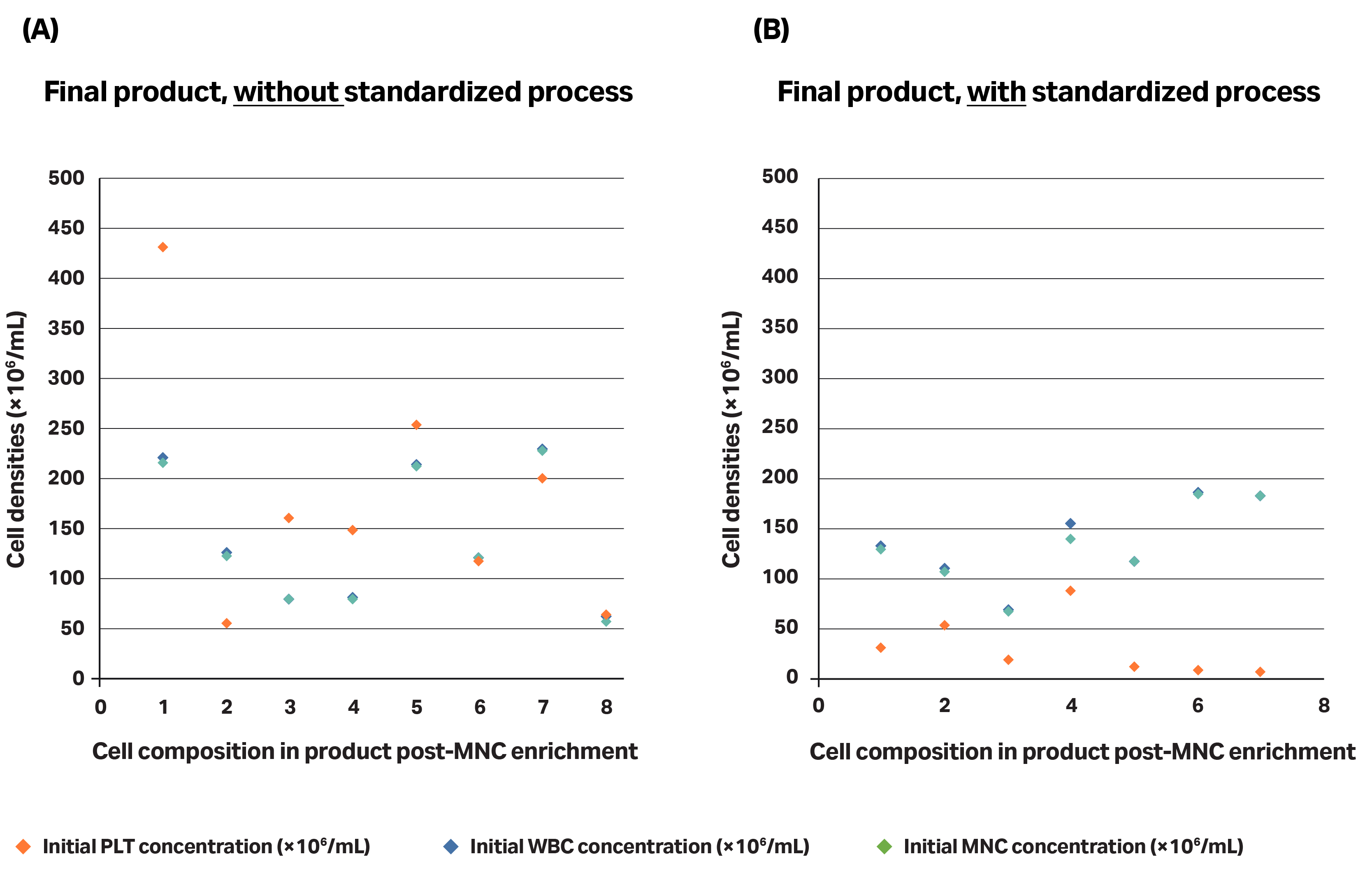
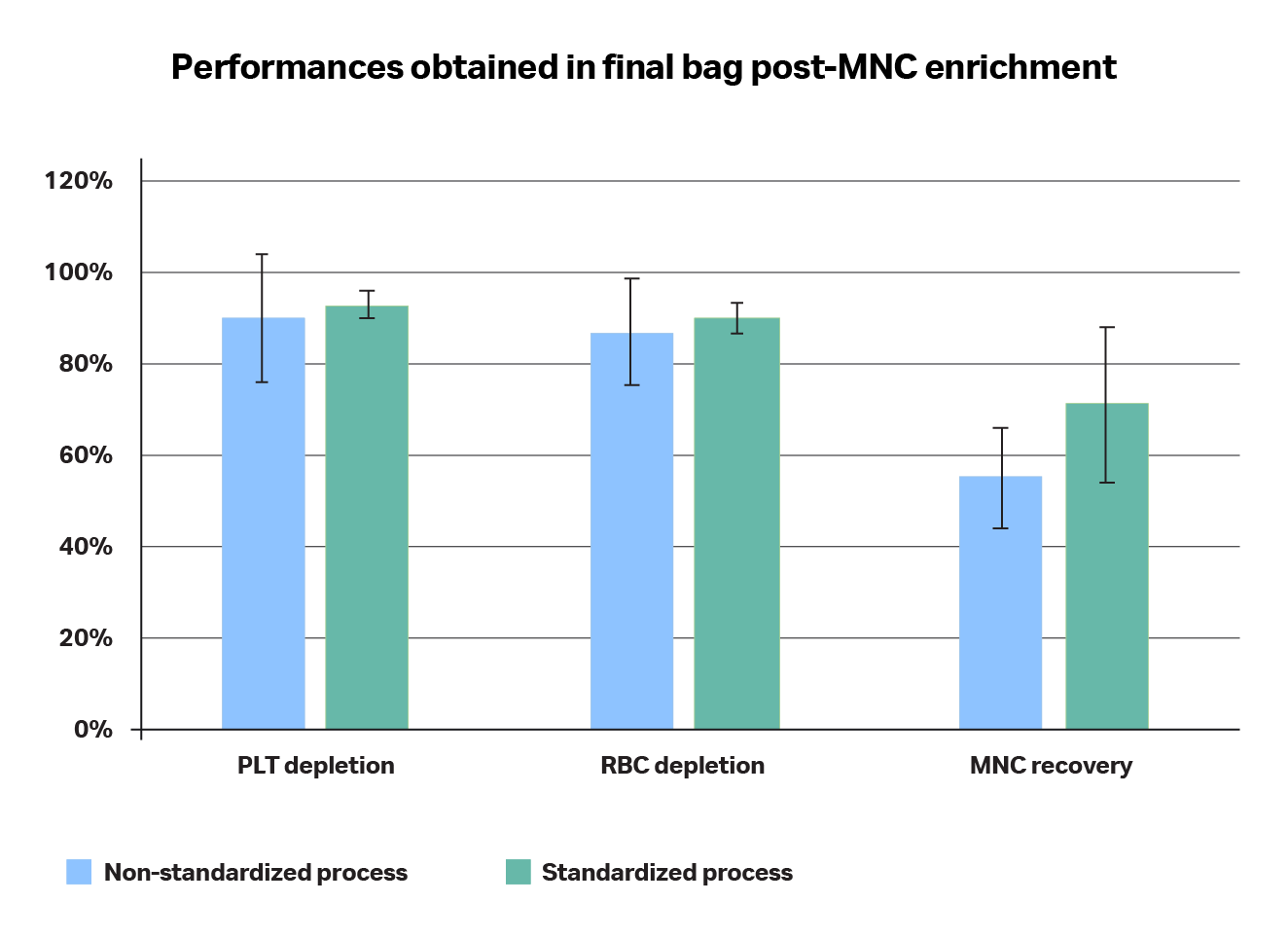
图 6.采用 (A) 或不采用 (B) 标准化流程获得的产品比较(针对细胞成分重新分布情况)。(A) 非标准化流程未遵循建议的运输条件,而是直接进行红细胞分离而未预先进行血小板去除,而 (B) 标准化流程包括:推荐血液成分分离制品的采集和运输条件以及血小板去除,然后进行红细胞分离。
图 7.比较使用非标准化 (A) 流程和标准化 (B) 流程时红细胞和血小板去除以及 MNC 回收方面的性能。非标准化流程的标准差显著高于标准化流程,且采用标准化流程时性能系统性更优。
MNC 富集步骤/工作流程的自动化
为 MNC 富集步骤制定标准流程后,需控制手动开放处理可能导致的操作人员误差和污染风险。为应对这一挑战,我们开发了自动化和功能性封闭式流程。根据初始产品是新鲜的还是冷冻保存的血液成分分离样本,可应用多种自动化解决方案(表 2)。
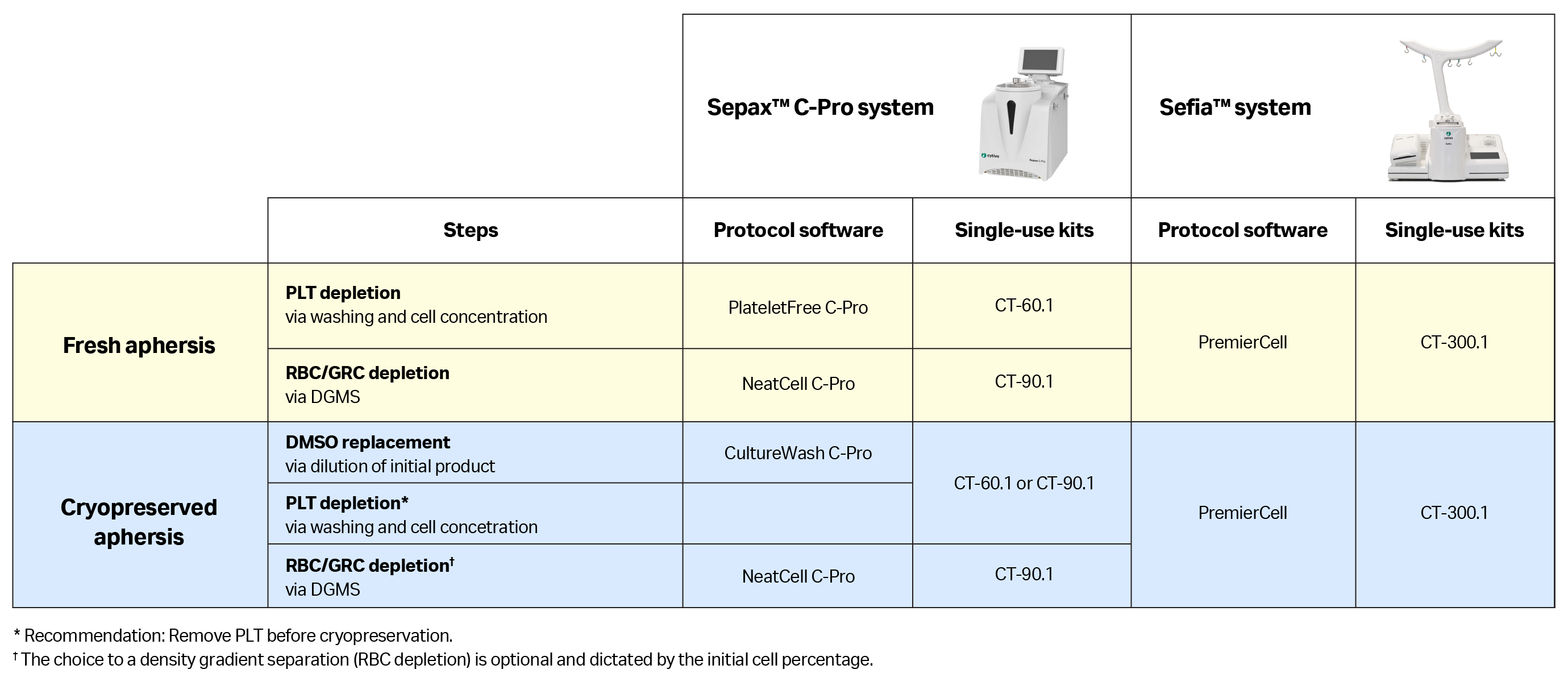
- 为 MNC 富集步骤制定标准流程后,需控制手动开放处理可能导致的操作人员误差和污染风险。为应对这一挑战,我们开发了自动化和功能性封闭式流程。根据初始产品是新鲜的还是冷冻保存的血液成分分离样本,可应用多种自动化解决方案(表 2)。Sepax™ C-Pro 细胞处理系统实现自动化和封闭式操作,使用 PlateletFree C-Pro 和 NeatCell C-Pro 应用程序及其专用一次性试剂盒进行连续两次操作。如果需要在单次操作中完成这两个步骤,可以使用Sefia™ 系统PremierCell 协议软件及其专用一次性试剂盒。
- 使用冷冻保存的血液成分分离样本时,需要额外进行稀释步骤,以替换细胞内所含冷冻保护剂溶液,并避免其在室温下产生毒性作用。稀释完成后,即可去除血小板、RBC 和 GRC。需注意,血小板去除通常在冷冻保存样本前进行,且红细胞计数可能足够低,无需使用密度梯度培养基进行特定分离
(表 2)。
表 2.新鲜或冷冻保存产品自动化 MNC 富集的解决方案汇总,包括设备、一次性试剂盒和协议软件
借助表 2 中概述的解决方案组合,我们可以实现 MNC 富集过程的标准化和自动化,尽管起始血液成分分离材料的细胞组成在不同患者之间存在差异。
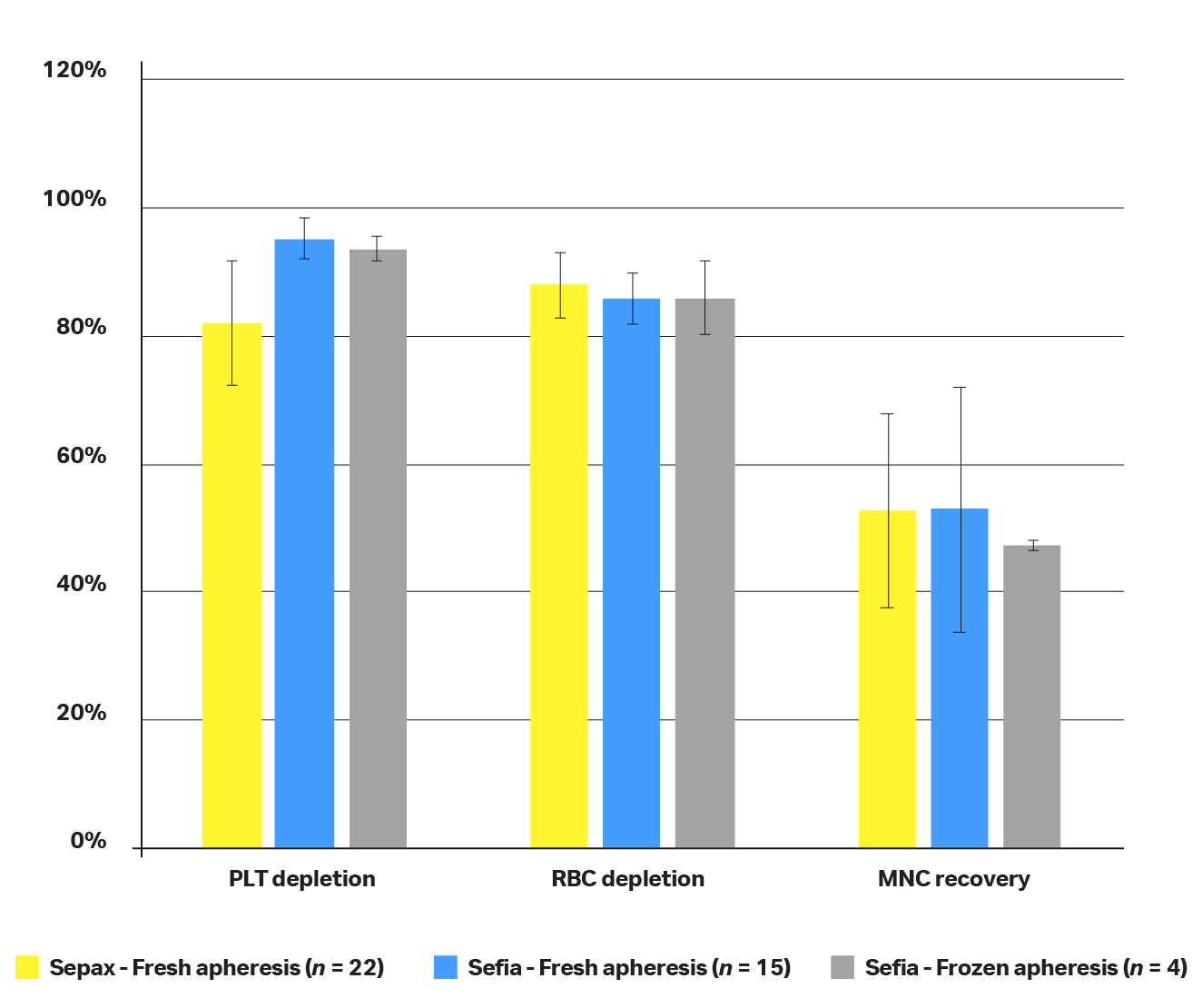
图 8.使用新鲜或冷冻输入产品时 Sepax™(黄色)和 Sefia™(蓝色)仪器的性能比较。数据来自 Sefia™ 和 Sepax™ 仪器处理的不同捐赠者的白细胞分离制品:来自 n = 22 名不同捐赠者的白细胞分离制品用于在 Sepax™ 仪器上生成性能数据,来自 n = 15 名不同捐赠者的白细胞分离制品用于在 Sefia™ 仪器上生成性能数据,来自 n = 4 名不同捐赠者的白细胞分离制品用于在 Sefia™ 仪器上生成性能数据(使用冷冻输入白细胞分离制品)。
已进行 F 检验和 t 检验以:
- 验证 Sepax™ 和 Sefia™ 数据集之间的方差齐性(分别采用新鲜和冷冻血液成分分离制品作为起始样本)
- 验证以新鲜血液分离制品作为起始样本时,Sefia™ 和 Sepax™ 仪器的 RBC/PLT 去除和 MNC 回收性能是否相当(表 3)
- 验证在 Sefia™ 仪器上,以新鲜 vs 冷冻血液成分分离制品作为起始样本时,RBC/PLT 去除和 MNC 回收性能是否相当(表 4)
F 检验表明,Sefia™ 和 Sepax™ 仪器在 RBC/PLT 去除或 MNC 回收方面的方差不齐(无论以新鲜还是冷冻血液成分分离制品作为起始样本)。
基于此结果,首先进行了一项假设方差不齐的 t 检验,比较了 Sepax 和 Sefia 仪器以新鲜白细胞分离制品作为起始样本时的性能。结果(表 3)表明:
- 以新鲜血液成分分离术制品作为起始样本时,Sepax™ 和 Sefia™ 仪器在血小板去除方面不相当——使用 Sefia™ 仪器获得的结果显示血小板去除比 Sepax™仪器高出 10% 以上
- Sepax™ 和 Sefia™ 仪器在红细胞去除方面相当
- Sepax™ 和 Sefia™ 仪器在 MNC 回收率方面相当
零假设:性能相当
表 3.以新鲜血液成分分离术制品作为起始样本时,假设 Sepax™ 和 Sefia™ 仪器之间方差不齐的统计检验
|
t 统计量 |
双尾 t 临界值 |
结果 |
结论 |
||
|
PLT 去除 |
-4.742822367 | 2.144786688 | t 统计量 < -="" /> t 临界值 |
拒绝零假设 → 均值不相当 | |
|
RBC 去除 |
1.148178789 | 2.055529439 | t 统计量 > - t 临界值 |
接受零假设 → 均值相当 | |
|
MNC回收率 |
-0.038254698 | 2.119905299 | t 统计量 > - t 临界值 |
接受零假设 → 均值相当 |
第二次 t 检验,假设方差不齐,比较 Sefia™ 仪器以冷冻和新鲜血液成分分离制品作为起始样本时的性能。结果(表 4)表明:
- 无论是以新鲜血样还是冷冻血样作为起始样本,PLT 和 RBC 的去除性能都相当
- • 无论是以新鲜血样还是冷冻血样作为起始样本,MNC 回收性能都相当
零假设:性能相当
表 4.以冷冻和新鲜血液成分分离制品作为起始样本时,假设 Sefia™ 仪器方差不齐的统计检验
|
t 统计量 |
双尾 t 临界值 |
结果 |
结论 |
|
|
PLT 去除 |
1.34217165 | 2.3060041 | t 统计量 > - t 统计量 > - |
接受零假设 → 均值相当 |
|
RBC去除 |
-0.0248962 | 2.77644510 | t 统计量 > - t 临界值 |
接受零假设 → 均值相当 |
|
MNC回收率 |
1.02312526 | 2.22813885 | t 统计量 > - t 临界值 |
接受零假设 → 均值相当 |
结论
细胞疗法生产过程中对源材料的处理是影响最终治疗质量和有效性的关键步骤。用于 CAR-T 细胞疗法的血液成分分离制品具有极高的变异性,受多种参数影响,包括:所使用的采集设备、血液成分分离设备所使用的方案、进行采集的操作人员、血液成分分离制品的储存和运输温度,以及最重要的是患者的独特特征。因此,对所有我们控制的参数进行标准化至关重要。
为了最大限度地减少可能影响输入产品的各种变异性来源,我们根据已发表的研究和本报告中提出的研究,提供了一份建议清单,以帮助实现血液成分分离制品的全程标准化。
我们的建议清单包括:在不同操作中使用相同的血液成分分离采集设备,将血液成分分离制品于 4°C 下运输以保持细胞活力,以及标准化 MNC 富集过程。
MNC 富集步骤的成功对于 CAR-T 细胞疗法步骤(尤其是 T 细胞分离)的效率至关重要。因此,我们建议在流程开始时对血液成分分离制品进行系统性富集,首先使用密度梯度培养基去除血小板,然后去除红细胞。
为了最大限度地减少程序和操作人员间的差异、避免污染并确保可追溯性,我们强烈建议在所有细胞疗法步骤(包括 MNC 富集)中尽可能使用封闭式自动化仪器。封闭式自动化处理将显著缩短生产时间,并确保这些敏感、关键疗法生产过程中必不可少的可追溯性。
参考文献
- Watson Douglas, Parrington J, Dowsing C, et al. Initial Comparisons of Three Apheresis Platforms for Supporting the Collection of CD3+ Cells for CAR-T Production. Cytotherapy. 2016. 18. S11. 10.1016/j.jcyt.2016.03.028.
- Clarke D, Taylor B, Lawrence N. A Comprehensive Analysis of Fresh Apheresis Collections: Conclusions and Best Practices (White Paper). HemaCare Corporation. WP-APH-BEST-PRAC-V1.0. Accessed 2021 Jun 23.
- López‐Pereira, P, Sola Aparicio, E, Vicuña Andrés, I, et al. Retrospective comparison between COBE SPECTRA and SPECTRA OPTIA apheresis systems for hematopoietic progenitor cells collection for autologous and allogeneic transplantation in a single center. J Clin Apher. 2020; 35: 453– 459.
- AABB Standards for Blood Banks and Transfusion Services, 32th Edition. http://www.aabb.org/sa/standards/Pages/standards-programs.aspx. Effective July 1, 2020. Accessed October 29, 2020.
- Mathur G, Mott SL, Collins L, Nelson GA, Knudson CM, Schlueter AJ. Factors influencing platelet clumping during peripheral blood hematopoietic stem cell collection. Transfusion. 2017;57(5):1142-1151.
- Brosig A, Hähnel V, Orsó E, Wolff D, Holler E, Ahrens N. Technical comparison of four different extracorporeal photopheresis systems. Transfusion. 2016 Oct;56(10):2510-2519. doi: 10.1111/trf.13728. Epub 2016 Jul 26. PMID: 27456672.