腺相关病毒 (AAV) 是一种日益常见的将核酸导入活细胞的载体,科学家主要将其应用于基因治疗。
标准的滴度分析方法为酶联免疫吸附试验 (ELISA),但该方法需要大量人工操作,且在精确度和重复性方面存在一定挑战。
在本应用说明中,我们介绍了基于表面等离子共振 (SPR) 技术的两种用于腺相关病毒 (AAV) 滴度分析的检测方法,分别针对血清型 2 和血清型 5。两种方法均能提供可重复的结果,并与传统的 ELISA 总 AAV 衣壳滴度分析方法具有良好的相关性。与 ELISA 相比,Biacore™ 检测具有更高的自动化程度和精确性,且可兼容从细胞收获液到最终纯化原液的各阶段工艺样品。其卓越的性能和简便的使用流程使其成为工艺开发的理想工具。
我们让病毒颗粒与共价偶联在 Biacore™ 传感器芯片上的 AAV2 特异性抗体结合,评估了 AAV 血清型 2 (AAV2) 的滴度。
我们让病毒颗粒与预功能化 Biacore™ 传感器芯片上捕获的 AAV5 特异性抗体结合,评估了 AAV 血清型 5 (AAV5) 的滴度。两种检测方法均使用 Biacore™ T200 SPR 系统开发,但也可在任何支持浓度分析的 Biacore™ SPR 系统上使用。
引言
病毒颗粒可以将外源核酸导入活细胞中,因此被视为传递遗传物质的合适载体。病毒载体在疫苗和治疗性应用(如基因治疗、细胞疗法、溶瘤腺癌症免疫疗法和肿瘤疫苗)中展现出广阔前景。常见的病毒载体系统包括腺病毒、腺相关病毒和慢病毒。
腺相关病毒 (AAV) 在基因治疗中已成为一种日益常见的载体。科学家在 20 世纪 60 年代将 AAV 识别为一种独立病毒类型,此前人们误以为其是腺病毒制备中的杂质。这种病毒不会引起疾病,仅会导致轻微感染。AAV 是一种体积较小的病毒,这也限制了其作为载体可包装的核苷酸序列长度 (< 4.4="" kb)。目前仍有研究致力于提高="" aav="" 的包装能力【参考资料="" />
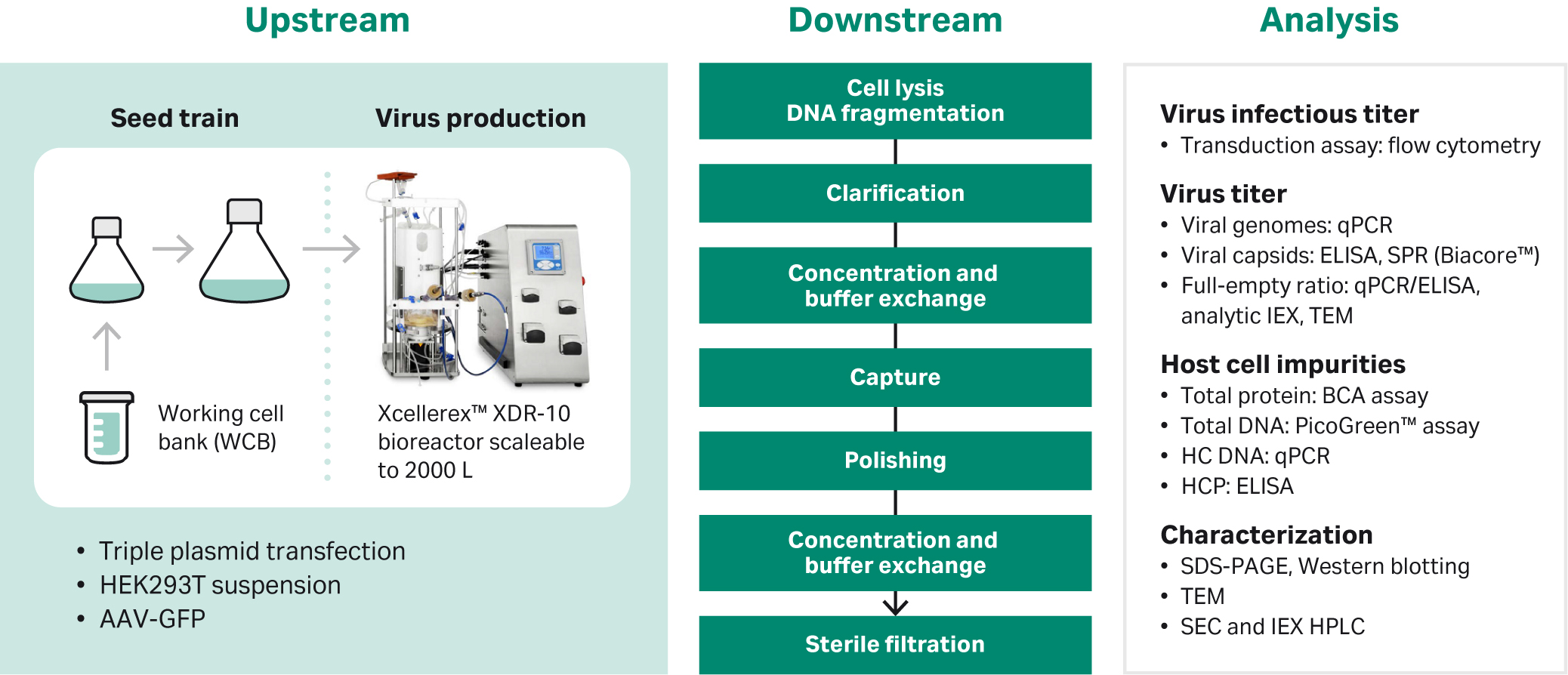
本应用说明涵盖了我们针对 AAV 血清型 5 从上游生产到最终纯化产物所开发的完整腺相关病毒生产流程中的分析部分。图 1 展示了该生产与纯化方案的说明。如需了解更多详细信息,请参阅参考文献 2、3、4 和 5。
图 1.AAV5 的生产与纯化方案。
在工艺开发、最终生产和纯化过程中,我们监测多种关键质量属性,包括感染滴度、病毒基因组滴度、病毒总颗粒数、宿主细胞蛋白和 DNA 含量。用于这些分析的许多技术涉及繁琐的人力流程、自动化程度低、精确性有限,且通常耗时且成本较高。
简化且高精度的分析方法,如 SPR,可通过高度自动化来优化当前工作流程。本文采用 SPR 技术对 AAV2 和 AAV5 进行总滴度分析。这两种方法均基于病毒颗粒与完整病毒颗粒特异性抗体的结合反应。
材料和方法
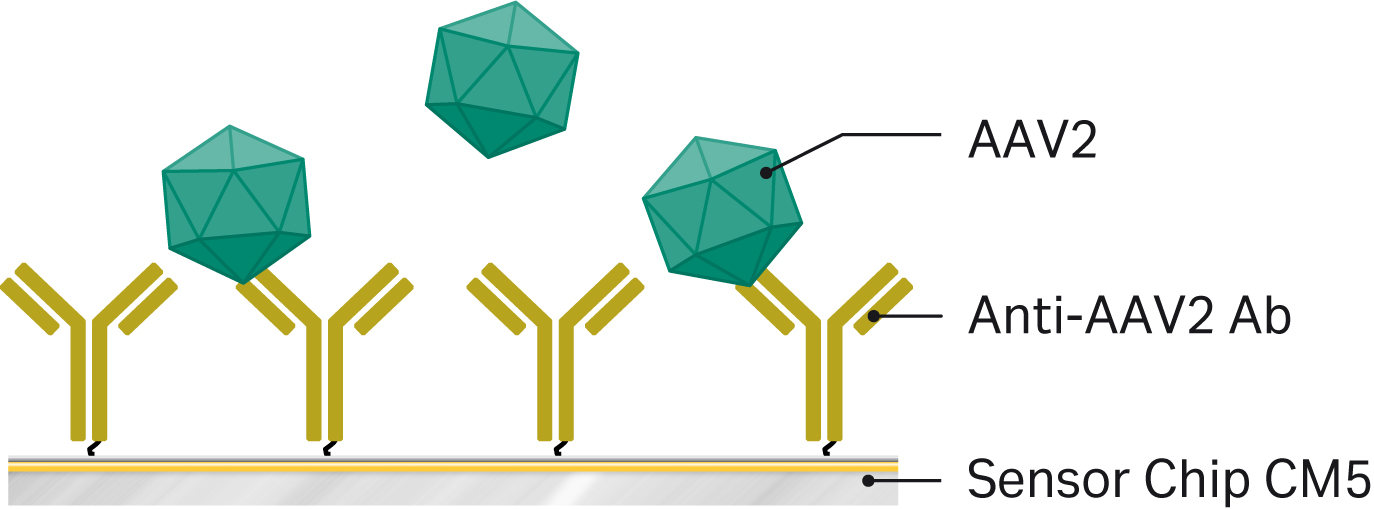
我们使用 Biacore™ T200 系统开发了用于 AAV2 总病毒颗粒滴度的分析方法。不过,凡是支持浓度分析的 Biacore™ 系统均可使用该方法。图 2 展示了该方法的原理。
图 2.使用 Biacore™ 系统进行 AAV2 滴度分析的原理图。将抗 AAV2 抗体通过胺偶联方式固定在 Biacore™ T200 中 CM5 传感器芯片的一个流通池中。随后将用含额外 NaCl 的流动缓冲液稀释(5 至 1000 倍)后的 AAV2 样本注射至表面,通过校准曲线计算病毒滴度。
我们将 Progen 提供的抗 AAV2 抗体(货号 610298)以标准胺偶联方式固定至 CM5 传感器芯片,使用 HBS-EP+ 作为运行缓冲液。抗体稀释浓度为 20 µg/mL,缓冲液为 10 mM 醋酸盐 (pH 5.0),注射时间为 7 分钟,最终偶联量介于 6000-10000 RU。偶联在 25˚C 下的单个流通池中完成。
在滴度分析中,使用 HBS-EP+ 补加 NaCl(终浓度为 0.3 M)作为运行缓冲液和样本稀释液。补加 NaCl 可消除来自粗样本的非特异性结合。根据预期滴度水平,样本通常稀释 5-1000 倍,每次实验中包含每个工艺样本的两个不同稀释倍数。样本注射条件为:接触时间 400 秒,流速 10 µL/min。采用 3 M MgCl2注射 60 秒进行再生。分析在 25°C 下进行,样本舱温度设定为 10°C 以保持样本稳定性。根据 Biacore™ 浓度分析的推荐方法,本滴度分析未使用参考表面。
校准曲线基于 ATCC 提供的 AAV2 标准品(ATCC AAV2 参考标准品 VR-1616)构建,浓度范围为3.6 × 108 至 9.2 × 1010 VP/mL,以2倍梯度稀释。在样本注射前设置第一条校准曲线,在样本注射后设置第二条校准曲线。该检测方法包含 5 至 10 个缓冲液和再生启动循环。
滴度检测中使用的抗 AAV2 抗体仅特异性识别完整的病毒颗粒。这意味着该检测可用于监测粗细胞培养样本中的 AAV2 滴度,且不会受到游离病毒或宿主细胞蛋白的干扰。根据供应商的规格说明,该抗体对 AAV3 也具有特异性,这意味着经过标准品、再生条件、接触时间、校准范围及其他参数的优化后,该检测同样适用于该血清型的分析。
AAV5 滴度分析
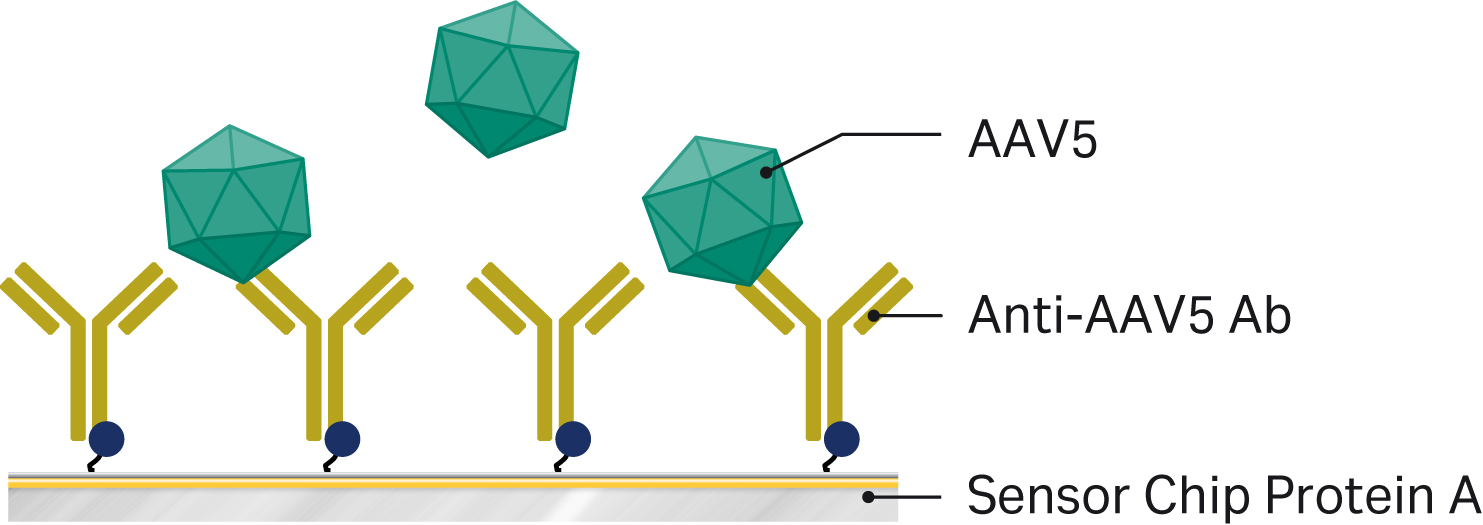
AAV5 病毒滴度分析同样使用 Biacore™ T200 系统进行。该检测基于传感器芯片蛋白 A 上的抗体捕获形式,无需单独的抗体固定步骤。我们选择捕获方式而非共价偶联,是因为我们的早期测试已表明本检测所用抗体 对酸性 pH 较为敏感,而胺偶联步骤通常需要在酸性缓冲液中进行,这样一来就将胺偶联排除。相比之下,捕获过程在中性 pH 下进行,对抗体更为温和。图 3 展示了该方法的原理。
图 3.使用 Biacore™ 系统进行 AAV5 滴度分析的原理图。抗 AAV5 抗体被捕获在 Biacore™ T200 的传感器芯片蛋白 A 中的一个流通池中。随后将用含额外盐分的流动缓冲液稀释(5 至 1000 倍)后的 AAV5 样本注射至表面,通过校准曲线计算病毒滴度。
我们将 Progen 提供的抗 AAV5 抗体(货号 610148)用流动缓冲液稀释至 16 µg/mL,并捕获至芯片的单一流通池中,再注入 AAV5 病毒样本。捕获步骤在 5 µL/min 的流速下进行,接触时间为 240 秒。
样本注射步骤的接触时间为 120 秒,流速为 10 µL/min。采用 pH 1.5 的 10 mM 甘氨酸-HCl 缓冲液注射 30 秒进行再生,取出芯片表面的捕获抗体与病毒。每个循环都捕获新鲜抗体。为保持样本稳定,样本舱温度设为 10°C,检测温度为 25°C。流动和样本稀释缓冲液为 HBS-EP+,并补充 NaCl 至 500 mM 的终浓度。根据预期滴度,样本稀释倍数为 10 至 1000 倍不等,通常每个样本使用两种不同的稀释倍数进行分析。我们使用 Vigene Bio 的 pAV-CMV-GFP (Full) AAV5(货号 CV10005)作为标准品,构建范围为1.7 × 1010 至 5.8 × 1011 VP/mL的校准曲线。检测流程包含 5-10 个缓冲液与再生启动循环,样本检测前后各运行一次校准曲线。
用于本检测的抗 AAV5 抗体仅识别完整病毒颗粒,使得该方法适用于细胞培养样本的分析,不会受到游离病毒或宿主细胞蛋白的干扰。
AAV 上游与下游样本
我们从上游生产与下游纯化流程的不同步骤中采集样本,样本基质和预期滴度差异较大。请参阅图 1 了解更多详细信息。
结果与讨论
AAV2 滴度分析
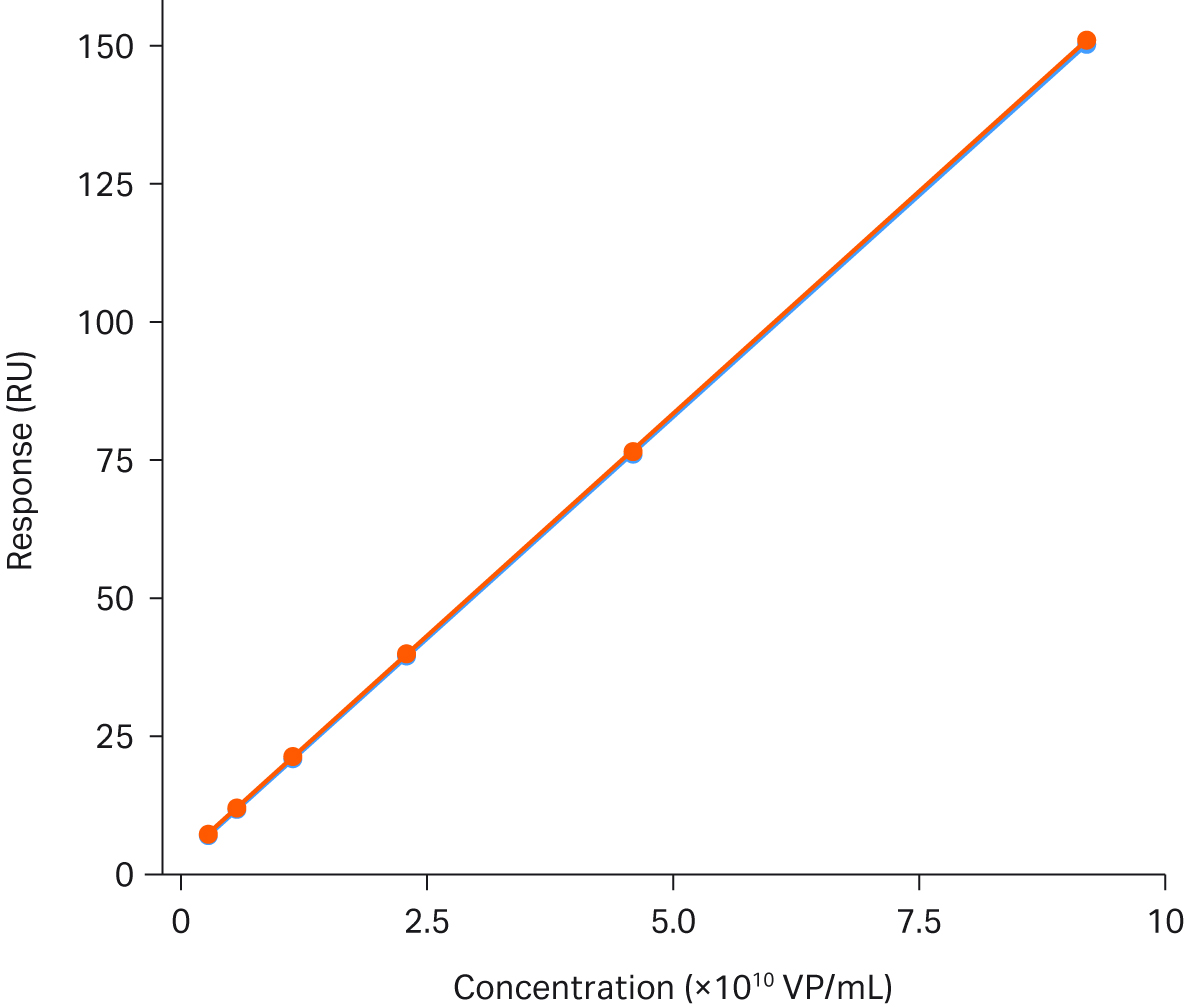
检测稳定性图 4 展示了 AAV2 滴度检测的稳定性。该图展示了两条校准曲线的完美叠加,期间进行了 66 个样品的检测。
图 4.使用 Biacore™ T200 进行 AAV2 滴度分析。该图展示了两条校准曲线的叠加,期间进行了 66 个样品的检测。校准曲线范围为 3.6 × 108 至 9.2 × 1010 VP/mL.
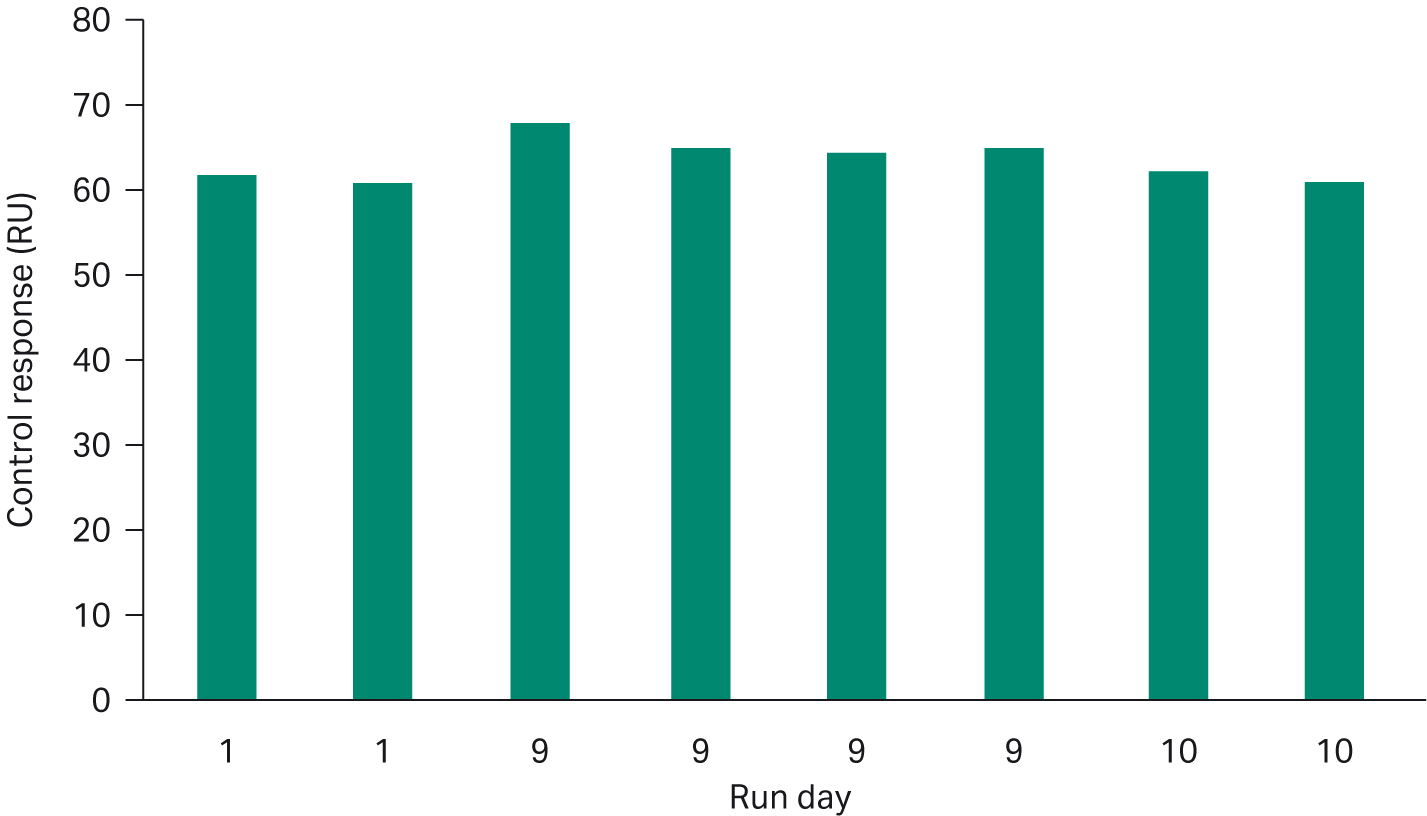
在方法开发过程中,我们发现该固定化芯片在推荐的运行条件下至少连续 10 天多次使用仍具有良好稳定性。其高稳定性支持“主校准曲线”方案,即在第 1 天运行一条校准曲线,并用于后续的样品检测。我们通过每次实验中加入内部阳性对照样品,持续监测固定化芯片性能。图 5 展示了使用同一固定化传感器芯片在 10 天内三次独立实验中阳性对照的响应水平。该对照响应水平的相对标准偏差小于 4%。采用主校准曲线可节省昂贵标准品用量并缩短检测时间。
图 5.10 天内三次独立检测中阳性对照的响应水平,均使用同一固定化传感器芯片。对照重复测量的相对标准偏差低于 4%。
标准品稳定性AAV2 ATCC 标准品以干冰冷冻 500 µL 分装形式寄送,收到后存储于 -80°C。首次使用时,我们将 ATCC 标准样品瓶解冻并分装为 15 µL 等分试样,储存在 Protein LoBind Eppendorf 样品瓶中。将等分试样继续保存在 -80°C。每次检测均使用新解冻的 15 µL 等分试样。
尽管小心操作,ATCC 等分试样活性随时间逐渐下降,表现为校准曲线响应范围降低。同期内,内部阳性对照的响应水平无显著变化。标准品活性和反应水平的降低导致样品病毒滴度估计偏高。我们在一次检测中对比了分装保存的 ATCC 标准品批次与新解冻的标准品批次。新批次标准品的响应水平是旧批次的两倍,证实旧批次标准品的活性已经下降。
该稳定性问题很可能是由于操作不当,在从冷冻柜取用标准品进行分析时发生了意外的冻融所致。通过更加规范的操作并尽量减少标准品暴露在室温下的时间,可显著延长其使用寿命。为了获得高性能的分析结果,始终妥善处理 ATCC 标准品至关重要。
AAV2 滴度分析的 LOD 和 LOQ我们根据阴性收获样本的背景信号计算了检测限 (LOD) 和定量限 (LOQ)。我们在连续三次运行中,对一个阴性样本进行十次重复测量,计算其平均响应值和标准偏差。然后,我们分别按照“平均值 + 3 × 标准偏差”和“平均值 + 10 × 标准偏差”的公式,计算了 LOD (RU) 和 LOQ (RU)。通过读取标准曲线,我们估算出 LOD 和 LOQ 分别约为2 × 109 VP/mL 和 5 × 109 VP/mL
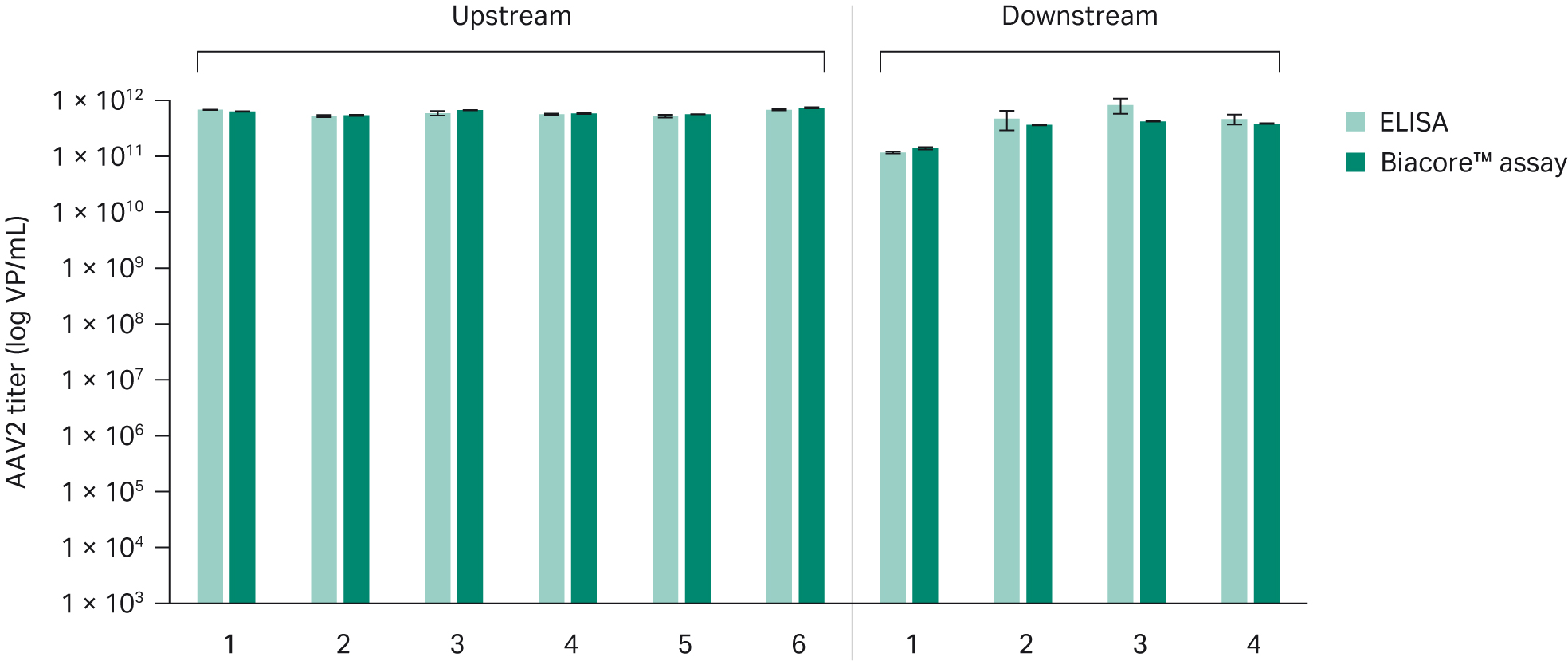
与 ELISA 的比较我们将 Biacore™ AAV2 滴度检测方法与 ELISA(Progen AAV2 滴度 ELISA,货号 PRATV)进行了比较。我们对上游收获样品和下游工艺样品均进行了分析。结果显示,Biacore™ 测定法与 ELISA 结果具有良好相关性。Biacore™ 测定法的组内精密度为 3%,明显优于 ELISA 的 ≥20% 精密度。
图 6.ELISA 与 Biacore™ 测定法在上游和下游样品中 AAV2 滴度测定结果的比较。
使用 Biacore™ 8K 进行 AAV2 滴度分析我们在 Biacore™ 8K 系统上建立了该测定方法,该系统显著提高了样品通量。
Biacore™ 8K 配备了八个通道,每个通道有两个串联的流通池,并配备八根并行操作的进样针。这种并行配置使得进行并行浓度分析成为可能。在并行浓度实验中,校准曲线分布在各通道上,每个通道对应一个校准点。这意味着,科学家只需一次循环即可完成校准曲线的运行,不同于串行设置需要在多个循环中分别运行各校准点。并行检测使用相同的校准曲线范围和接触时间。运行中加入标准化循环,用于补偿各通道之间的细微差异。出于实际考虑,标准化溶液可以选用某一个校准点。借助并行校准曲线以及八个样品的并行检测,该系统显著缩短了总体运行时间。对于整板 96 孔样品,该系统可将运行时间缩短至 3 小时以内,而使用单进样针系统则需约 19 小时。
图 7.Biacore™ 8K 可同时分析八个样品,显著缩短运行时间。
AAV5滴度分析
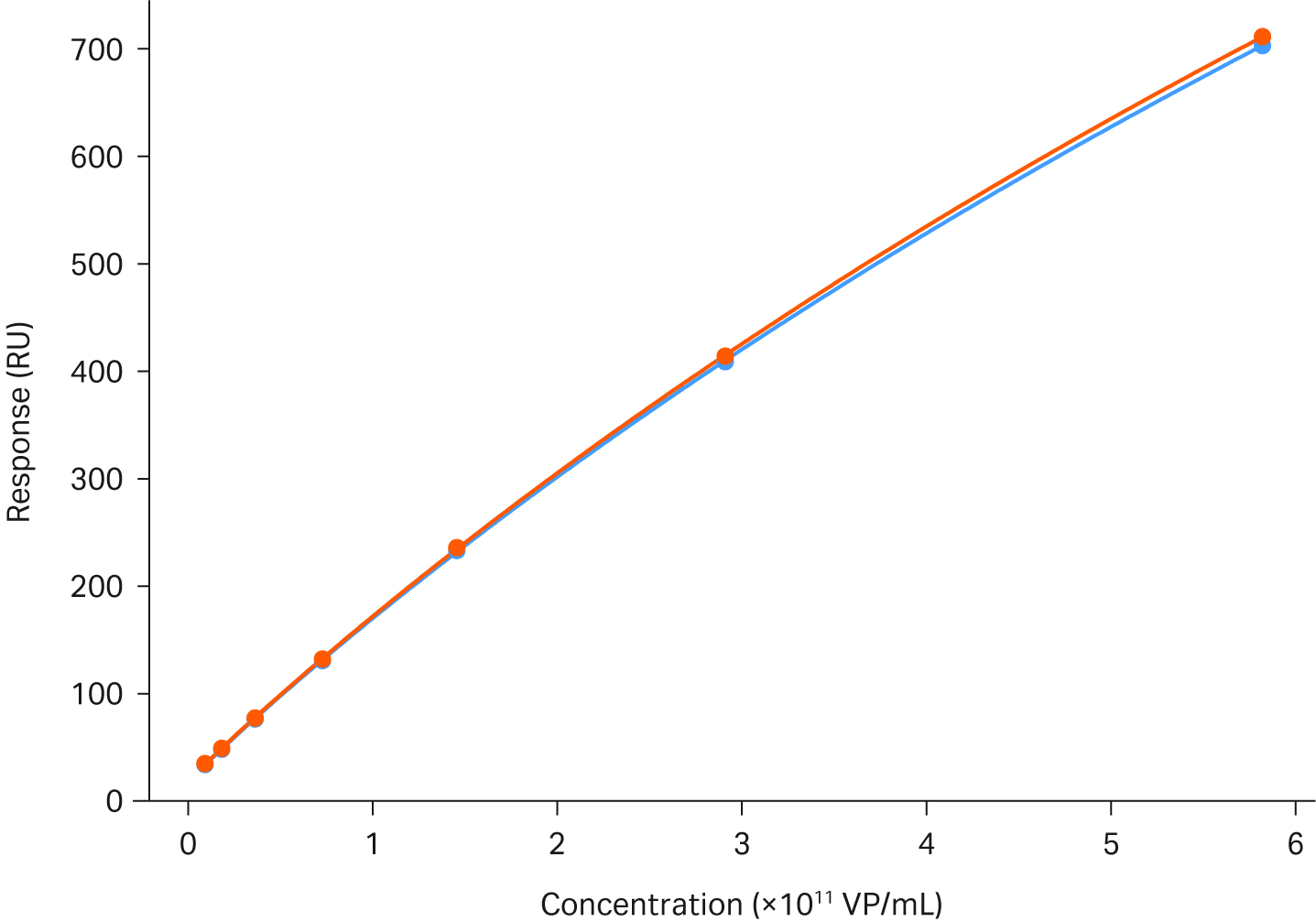
检测稳定性AAV5 滴度分析设置为捕获法,因此每个循环都需要捕获抗 AAV5 抗体。这种方式意味着每一循环都相当于使用了一个全新的表面,因此无法像 AAV2 滴度分析那样使用统一的校准曲线。不过,用于捕获抗 AAV5 抗体的传感器芯片蛋白 A 稳定性极高,可在多个实验中重复使用,且不会影响表面性能。图 8 显示了使用 Vigene 全长标准品获得的校准曲线。
图 8.使用 Biacore™ T200 进行 AAV5 滴度分析。该图展示了两条校准曲线的叠加,期间进行了 16 个样品的检测。校准曲线范围为 9.1 × 109 至 5.8 × 1011 VP/mL.
标准品稳定性
我们在 AAV5 分析中使用了 Vigene 全长标准品。我们将标准品分装为 25 µL 等分试样,储存在 -80°C。每次分析使用前,从冰箱中取出一个新等分使用。在整个项目过程中,未观察到该标准品存在稳定性或活性下降的问题。Vigene 标准品的温度敏感性似乎低于 AAV2 的 ATCC 标准品。
AAV5 滴度分析的 LOD 和 LOQ我们在连续三次运行中,对一个阴性样本进行十次重复测量,计算其平均响应值和标准偏差。然后,我们分别按照“平均值 + 3 × 标准偏差”和“平均值 + 10 × 标准偏差”的公式,计算了 LOD (RU) 和 LOQ (RU)。估算得出 LOD 和 LOQ 分别约为9.8 × 109 VP/mL 和 1.7 × 1010 VP/mL。
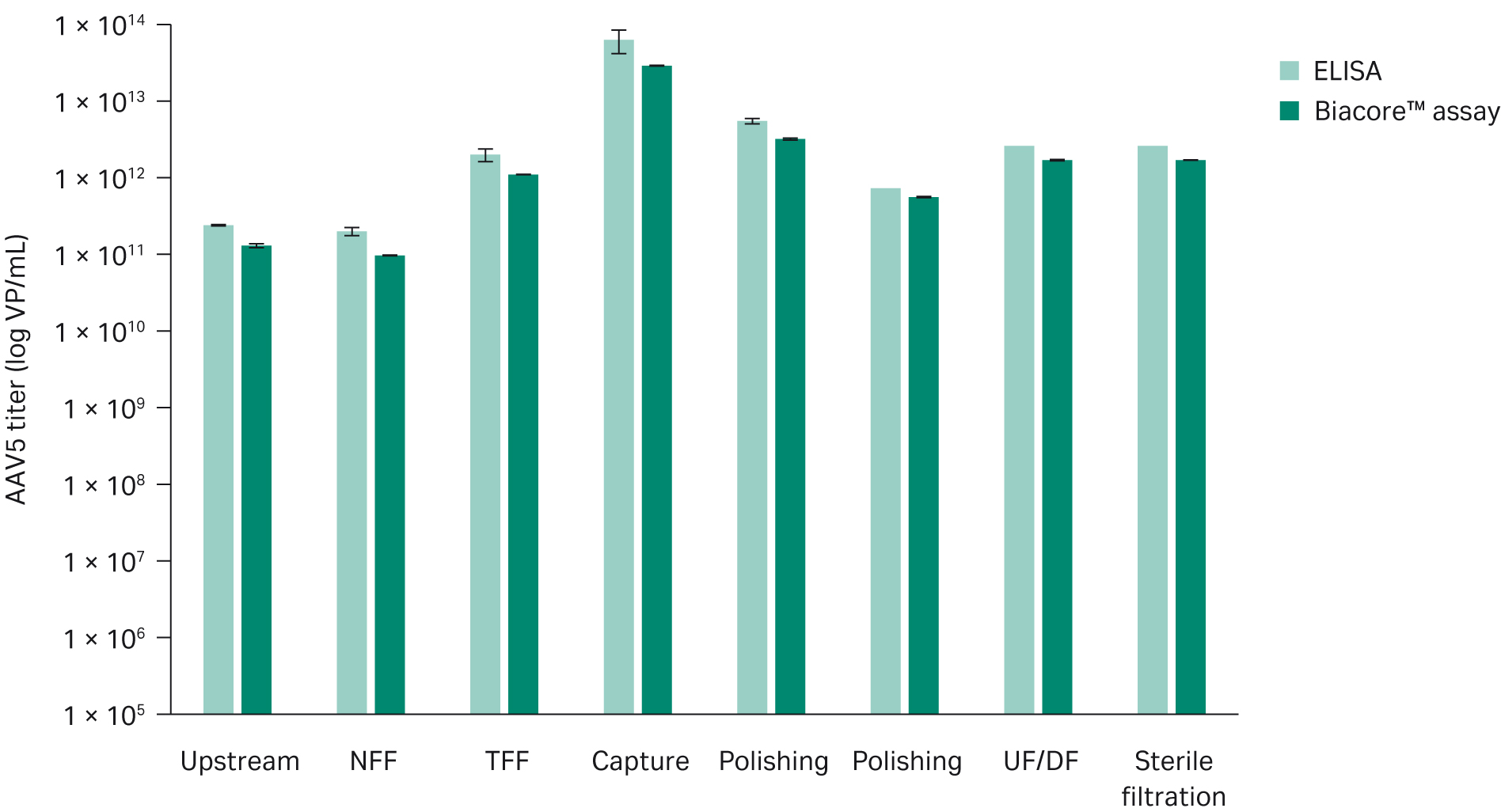
与 ELISA 的比较我们使用 Biacore™ 对一组 AAV5 工艺过程的上下游样品进行了分析,并将结果与 ELISA(Progen AAV5 Titration ELISA,货号 PRAAV5)进行了比较。两种方法的检测结果高度相关,但 Biacore™ 分析得出的滴度略低(图 9)。然而,两者之间的滴度差异较小,可能源于运行条件的差异。Biacore™ 分析经过优化以降低非特异性结合,而 ELISA 使用的是标准缓冲液条件。这意味着 ELISA 中可能存在一定程度的非特异性结合。
对于这一组样本,Biacore™ 分析的平均试验内精密度为 2%,而 ELISA 为 15%。
图 9.ELISA 与 Biacore™ 分析在不同 AAV5 上下游样品中的病毒滴度对比。ELISA 得出的滴度略高,可能是由于在 ELISA 板上产生了非特异性结合。
结论
Biacore™ AAV 滴度分析方法能够产生稳定且重复性高的结果,与采用 ELISA 的传统方法高度相关。与 ELISA 相比,Biacore™ 滴度分析的变异性显著更低。Biacore™ 分析流程自动化程度高,操作时间短,样品制备简便,数据结果分析自动完成。另一个优势是 Biacore™ 传感器表面可多次重复使用。对于 AAV2 的滴度分析,可以使用同一固定化传感器芯片进行至少 10 天的检测,配合主校准曲线,从而节省标准品和成本。用于 AAV5 分析的传感器表面 — 传感器芯片蛋白 A,同样具有很高的稳定性,可多次重复使用。
这两种分析方法均可应用于任何支持浓度分析的 Biacore™ SPR 系统。在 Biacore™ 8K 或 Biacore™ 8K+ 系统上运行该分析,可大幅提升样品通量并缩短总运行时间。Biacore™ 分析不仅是质量控制的优秀工具,同时也适用于工艺优化。
参考文献
- Choi, JH., Yu, NK., Baek, GC. et al. Optimization of AAV expression cassettes to improve packaging capacity and transgene expression in neurons. Mol Brain 7, 17 (2014). https://doi.org/10.1186/1756-6606-7-17
- Application note: Cell culture process development for AAV vector production in suspension cells
- Application note: Adeno-associated virus production in suspension HEK293 cells with single-use bioreactors
- Application note: AAV5 capture and polishing optimization
- Application note: AAV5 purification including analytics
- Article: Develop and refine your AAV production process
订购信息
| 产品信息 |
说明 |
货号 |
|---|---|---|
| S 系列 CM5 传感器芯片,3 片装 |
3片装 |
BR100530 |
| S 系列传感器芯片蛋白 A |
3片装 |
29127556 |
| 氨基偶联试剂盒 |
固定试剂 |
BR100050 |
| HBS-EP+ 缓冲液 10x |
分析缓冲液 |
BR100669 |
| 甘氨酸 1.5 | 再生溶液 |
BR100354 |
| 醋酸盐 5.0 |
偶联缓冲液 |
BR100351 |
| Biacore™ T200 |
用于分子相互作用表征的 SPR 系统 |
28975001 |
| Biacore™ 8K |
用于分子相互作用表征的 SPR 系统 |
29337763 |
| Biacore™ 8K+ |
用于分子相互作用表征的 SPR 系统 |
29283382 |