作者:Paul Belcher(Cytiva 产品战略经理)与 Martin Teichert(Cytiva 全球产品经理)
高人才流失率一直是困扰制药行业药物开发的难题。除此之外,美国新药研发的效率每过九年就会下降一半(Erooms Law)。1 这些因素综合作用的结果就是开发人员需要测试的样本更多,需要收集的信息更多,而做决策的时间更少。
为了应对需求变化,有必要在早期药物发现过程中引入能够提供丰富信息的技术。尽管目前有些数据分析工具已经得到改进,但开发人员仍然面临手动、耗时的问题,而且分析工具没有随着仪器通量的增加而扩展。
改变从现在开始。为了提高效率和生产力,科学家们开发了一种人工智能的分析方法,实现了基于机器学习的数据解决方案,可以优化药物早期高通量筛选和表征的分析方法。
信息海洋里轻松捞针
表面等离子共振 (SPR) 是科学家在药物发现全过程中连续使用的一种实时且能提供丰富信息的分析技术。SPR 技术可以检测和表征分子或化合物与靶标的结合,并提供有价值的亲和力和动力学参数信息。通过分析这些信息为药物决策提供指导,促进新药的开发和临床应用。
SPR 现已成为低分子量药物发现的重要工具。得益于出色的灵敏度,SPR可以检测和表征与靶标结合的低分子量和低亲和力化合物。SPR 不仅可以鉴定苗头化合物,还可对结合进行量化,因此科学家可以根据化合物的亲和力、动力学特性和配基效率对化合物进行排序和表征。这些信息对于“苗头到先导”开发过程中化合物结构确定工作具有非常重要的支持作用,可以帮助科学家进一步确定苗头化合物的化学结构和优化先导化合物。由于需要实时生物物理数据为决策提供支持,科学家们在药物发现过程中对于 SPR 平台的使用有提前化的趋势。
然而,目前光学生物传感器(如 SPR)的信息分析方法并未随着仪器通量的增加而扩展。目前数据分析仍然是一个手动、繁琐的过程,开发人员需要处理、理解和解释大量数据,非常耗时。
解决该问题的常规做法是提高劳动强度或增加人手。但这些解决办法是不可扩展的,并且会带来偏差和不一致问题。例如,无意视盲往往导致人们忽视非预期的情况。无意视盲发生在分析的数据量非常大的情况,使我们容易被过往分析的数据所影响或产生偏见。这种认知错觉的问题在于,即使我们意识到该问题存在也很难避免,而且会妨碍专家获得偶然和意外发现,导致错失制药行业的重大突破。
预期思维的可怕之处在于我们只会看到我们预期看到的问题。Alexander Fleming 爵士在介绍发现青霉素的过程时曾说过这样的话,“……我当时并没有指望通过发现全世界首个抗生素或灭菌剂来彻底改变整个医学领域。不过我认为我当时就是要彻底改变整个医学领域。”2 此外,Cytiva 的内部研究表明,在一天的不同时间点或不同分析日期,用户之间或同一用户的分析差异范围在 10% 至 30% 之间。
即使可以增加人手来解决该数据瓶颈问题并克服人固有的偏见,也需要投入大量的时间和资源进行人员培训。无论采用何种生物物理技术,生物物理数据分析的教育和培训都可能需要数周、数月乃至一年多的时间。我们的出路在哪里?
依靠 AI 解决方案
尽管使用数据分析可以解决部分问题,软件解决方案得到了改进,界面更加扁平化,数据更正与引用实现了自动化。然而这些改进并未完全解决数据瓶颈问题,无法显著提高日常工作效率。
人工智能的作用越来越明显,可以处理手动的、繁琐的步骤,减轻开发人员的工作量。但目前 AI 数据分析在药物发现领域的应用主要仅限于大容量图像分析。而在生物物理学领域,AI 的应用仅限于改进核磁共振和质谱的峰值检测。
AI 数据分析技术在药物发现中得不到充分采用的原因是多方面的,例如缺乏进行算法训练所需的大量高质量数据。再就是缺乏对 AI 技术的理解,公众不确定是否需要采用 AI 技术,Elon Musk 更是认为 AI 比核武器更危险。3 虽然 AI 计划算法比较简单,但其他 AI 技术却非常复杂。虽然可以通过方框图了解输入与输出之间的关系,但是对于中间实际发生的过程却知之甚少。
AI 技术有助于克服分析中的不一致问题,为开发人员节省时间,但该技术也将来自 SPR 的丰富数据简化为二进制运算,例如是或否,接受或拒绝,而对于决策过程却没有帮助。这就带来了一个新问题,那就是如果我们连决策如何做出的都不知道,如何能够信任决策?在药物发现中,忽视错误会导致我们继续研究错误甚至危险的化合物,并迫使我们在后期放弃候选药物。
透明化机器学习为我们提供了解决方案。透明化机器学习技术通过可视化与注释让我们了解算法输出的形成过程,从而帮助我们建立对于 AI 解决方案的信任。
Cytiva 的机器学习原型
Cytiva 正在开发可训练的原型机器学习解决方案,用于分析和表征 Biacore™ SPR 数据。我们的解决方案根据不同应用领域专家的数据评估需求通过一组特征或分类来定义模型。科学家可以根据需要随着研究的变化和进展对算法进行训练和调整。这种方法消除了手动操作,减少了错误并提高了一致性,可以减少分析数据所需的时间。我们的 SPR 团队对软件进行预训练,以帮助制定标准化的工作流程,并节省新用户培训时间。
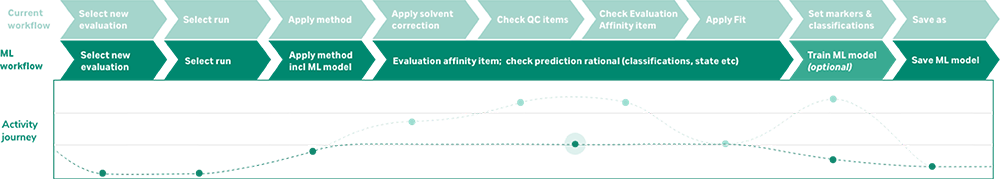
为了衡量和验证模型的性能,Cytiva 用一年的时间在用户工作地点部署了其解决方案。我们的结果表明,分析时间最高可减少 90%,每位合作者在每周多次运行的测定中,每次实验可节省 8 小时以上。通过消除拟合前后数据整理和可视化评估的耗时的手动操作,我们的透明机器学习原型帮助全行业开发人员取得了重大成果(图 1)。
图 1:使用 Cytiva 机器学习原型显著减少数据分析时间。
Cytiva 的合作者还发现,在分析大型数据集时,这种方法可以提高数据分析的一致性。与 Biacore™ 专家进行的分析相比,该原型发现的重合率达 95% 以上。节省出的时间可以让开发人员同时支持多个项目,运行更多生物物理分析,以提高他们对所开发化合物的信心。
由于只有 10% 的药物可以通过 I 期临床试验,因此我们必须设计并采用更有效的方法和技术来改进药物发现早期阶段的工作流程,以便将更优质的候选药物引入临床阶段。4 随着 AI 的进步(例如 Cytiva 的机器学习解决方案),一种更智能、更快速的方法来被用来获得结论性的结果,从而提高生产力,缩短获得结果的时间,并最终推进和加速新疗法的开发。
- Nosengo N., Can you teach old drugs new tricks?Nature. 2016;534:314–6.
- Tan, S. Y., & Tatsumura, Y. (2015).Alexander Fleming (1881-1955): Discoverer of penicillin.Singapore medical journal, 56(7), 366–367.https://doi.org/10.11622/smedj.2015105
- Clifford, C., Elon Musk: ‘Mark my words — A.I. is far more dangerous than nukes’ (2018).CNBC.https://www.cnbc.com/2018/03/13/elon-musk-at-sxsw-a-i-is-more-dangerous-than-nuclear-weapons.html
- Takebe, T., Imai, R., & Ono, S. (2018).The Current Status of Drug Discovery and Development as Originated in United States Academia: The Influence of Industrial and Academic Collaboration on Drug Discovery and Development.Clinical and translational science, 11(6), 597–606.https://doi.org/10.1111/cts.12577