随着数字化技术的发展,机理建模在生物制药行业获得了广泛关注。机理模型是一项非常具有前景的描述层析工艺的技术。这些模型具有众多优点,例如降低成本和时间,并且适用于产品生命周期的任何阶段。数字孪生基于机理模型,可以帮助深入了解非常复杂的分离问题。
然而,机理建模的主要缺点是模型校准方法比较繁琐。多组分原料由于存在许多未知的蛋白参数,容易导致多维的参数估算问题。标准模型校准技术可能出现不合理的相关性和不切实际的物理参数估算。但是,我们如何同时降低这种风险,提高模型质量,并减少模型校准所需的时间呢?
1.设定范围
第一步是设定范围并定义项目目标。必须了解工艺挑战并定义预期的模型功能,以确保模型可以满足后续需求。这些考虑因素对于设计校准实验和定义模型验证策略都非常重要。
2.实验设计
首先需要定义模型的质量要求,其他还包括能力、资源和专业知识要求。之后才能确定合适的实验。校准实验需要特别注意两个问题。首先,实验质量对于消除不确定性因素极为重要(例如,未知孔隙率、系统死体积、离子结合载量等)。其次,校准实验需要有足够的可变性,以便获得模型应用所需的所有相关信息。
该阶段应该制定验证策略或大致验证策略。目的在于确保模型能够满足后期的设计意图。
3.选择模型
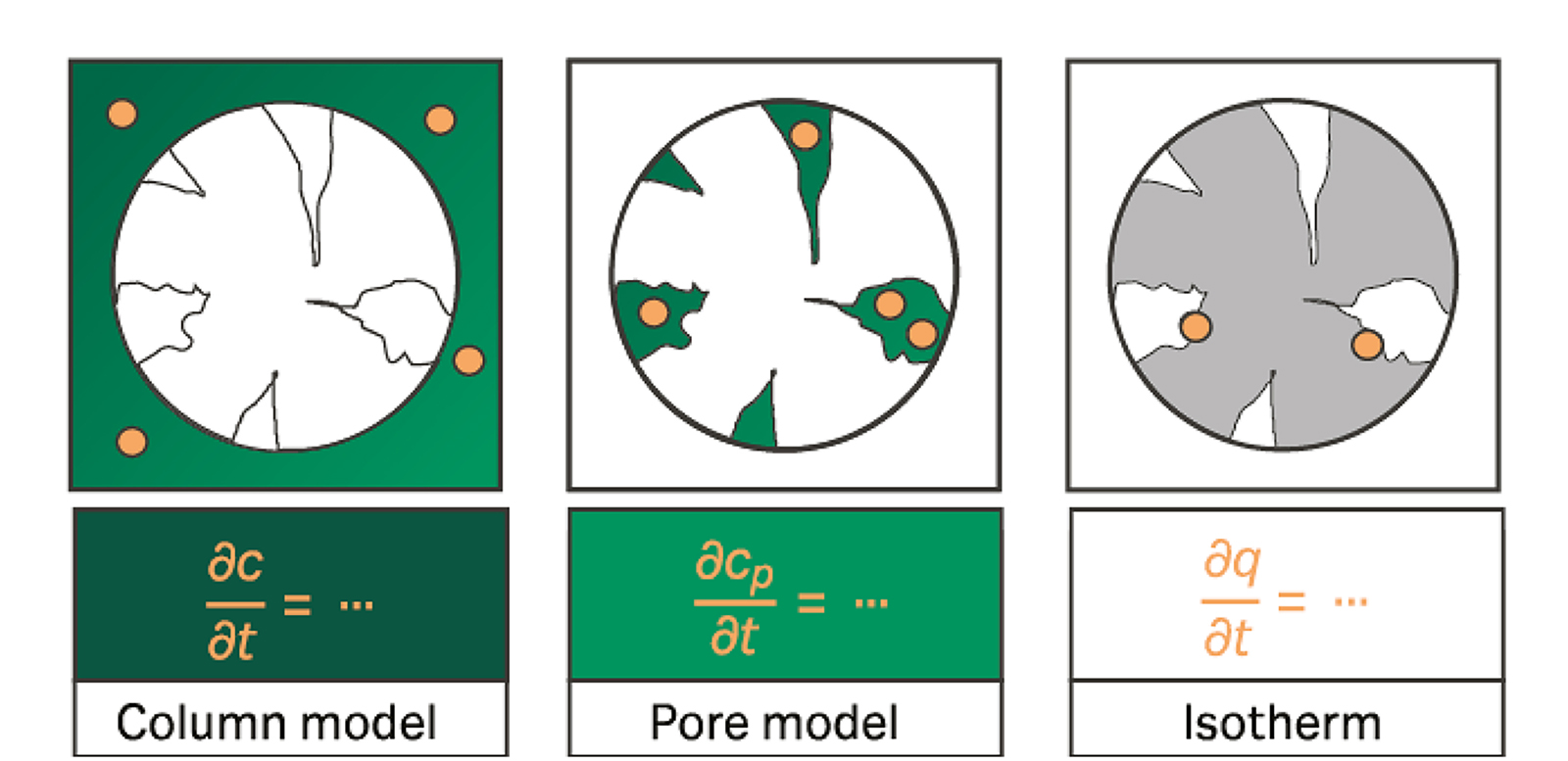
选择模型时,同样必须注意避免选择参数与当前项目不相关的复杂模型,导致增加不确定因素。除非有必要,尽量避免选择复杂的层析柱、孔和等温线模型。
4.检查输入数据
生成的数据需要先进行调查之后,方可用于模型校准。一定要考虑实验数据的特征,例如需要对反混效应进行建模。
5.校准模型
为了避免参数相关性失去实际意义和不合理的参数估算,模型校准工作流程最好采用自下而上的方法,即从简单的模型和少量校准实验开始,逐步增加复杂性。有些层析图谱特性可以提供一定的参数信息。最好利用这些特性来确定参数。
例如,Yamamoto 方法就是利用低柱载离子交换层析(IEX)线性梯度洗脱(LGE)来确定蛋白质电荷和平衡常数。该过程至少需要三个不同梯度长度的 LGE,才能根据梯度斜率和保留的盐浓度确定电荷和平衡常数。然后将获得的参数值转移到其他校准实验加以使用。Yamamoto 方法可以直接在 GoSilico™ 层析建模软件中实现。
确定电荷和平衡参数后,可以通过逐步洗脱确定其他参数,例如结合动力学、传质和孔扩散特性。由于蛋白质分子之间的空间位阻和排斥而产生的配基屏蔽,可以通过另外的高负载 LGE 来确定。这种逐步推进的方法可以降低不合理的相关性和不切实际的物理参数估算风险。
6.分析参数不确定性
机理模型校准后,需要调查模型质量。模型质量的第一个指标是视觉拟合度。高质量模型能够准确地描述所有的校准运行过程。
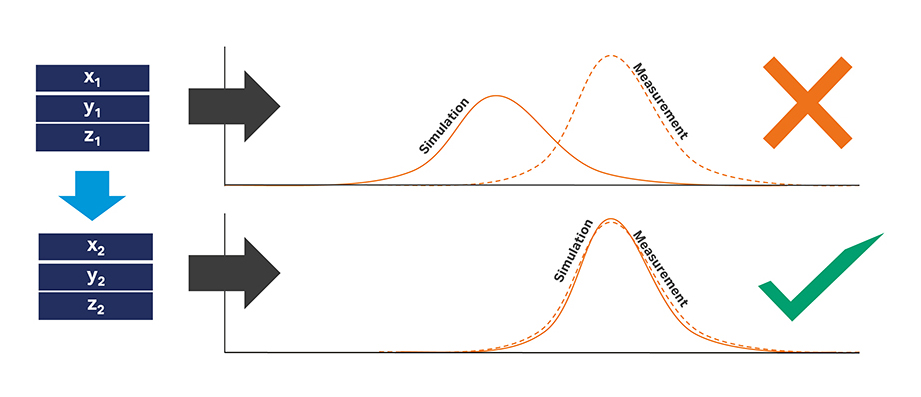
获得良好的视觉拟合度后,需对模型质量进行更严格的评估。为了研究参数敏感性,需要确定 95% 置信区间 (CI)。可以直接使用 GoSilico™ 层析建模软件计算 95% 置信区间。置信区间小 (CI) 说明选择的参数比较准确。CI 大表明无法通过校准数据准确地确定相关参数。
为了研究不敏感参数对质量属性(例如收率或纯度)的影响,可以在 CI 范围内进行参数空间采样,以此来确定参数是否足够敏感。然后根据参数不确定性分析结果继续进行校准实验,以提高模型质量。
7.验证模型
确定最终校准模型后,必须通过实验对模型进行验证。如前所述,验证策略应在实验设计阶段就已确定。模型验证可以通过一个或多个实验来完成。
常用的一种方法是通过数字模拟优化工艺条件进行模型验证。另一种方法是选择模型接近失效时的工艺条件。如果已对所有使用的系统和层析柱进行了表征,还可以在不同的规模下进行实验。每个校准的机理模型都应能够通过外推方式确定校准空间范围以外的工艺条件。
通常需要对峰形状和位置以及关键质量属性进行验证。可以将验证运行导入到 GoSilico™ 层析建模软件中来比较实验数据和预测模型。
8.应用和开发机理模型
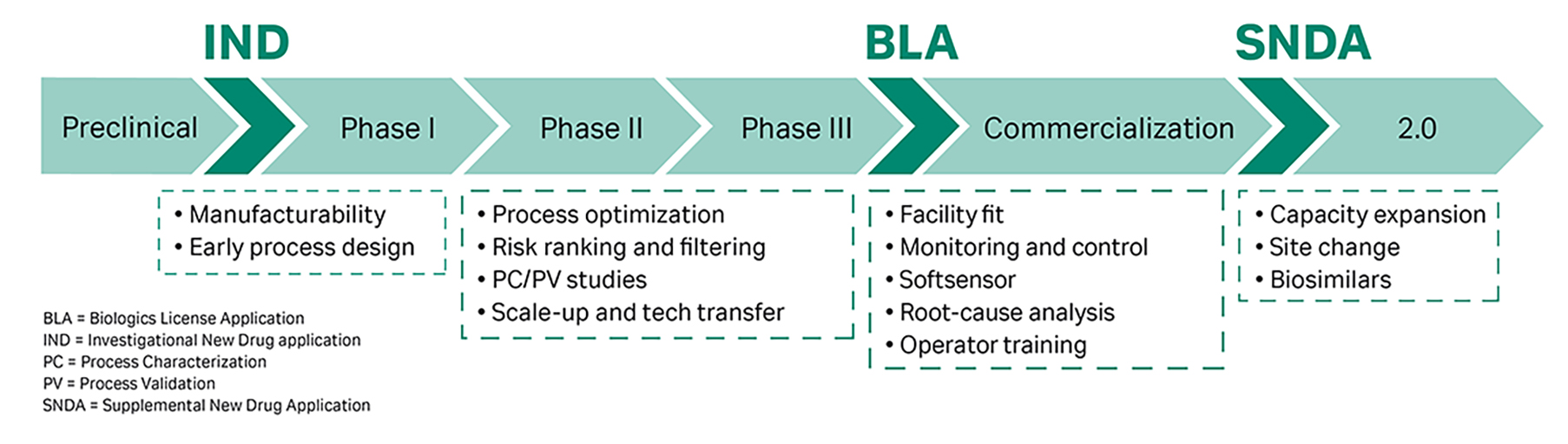
在成功校准和验证后,就可以在产品的整个开发生命周期中使用模型了。
由于不同的模型用途对于模型质量和功能有不同的要求,因此在整个建模过程中要时刻注意模型的用途,以确保获得合适的投入产出比。
总结
本次介绍的机理模型校准流程清楚,简洁,机理模型校准非常方便,提高了校准速度,降低了模型的不确定性,同时降低了参数过拟合的风险。采用这种方法可以避免机理建模的主要缺点,充分发挥机理建模的潜力。