作者 Tobias Hahn 博士,Cytiva 思拓凡首席科学家
简介
最近数十年,计算机模拟已成为许多行业必不可少的工具。以汽车与航空航天业为例,模拟技术的运用大大缩短了创新周期,提高了生产力。化工行业也从该技术的发展中受益。尽管生物制药行业是一个创新性行业,但生物工艺开发领域却刚刚开始采用基于模拟技术的工作流程。
许多从事生物工艺行业的人士一致认为,仅靠成本高、耗时长的实验室实验、迭代性实证研究优化,甚至统计学方法,是无法应对未来挑战的。许多全球性生物制药公司已着手建立他们的上游或下游工艺数字孪生系统。监管机构鼓励发展此类技术:欧洲药品管理局 (EMA) 与美国食品药品监督管理局 (FDA) 早在质量源于设计 (QbD) 倡议中就提出了深入了解生产工艺的要求,当时明确提出,模型与计算机模拟是证明我们对机理过程的现有理解的最佳选择 (1)。
数字孪生的类型
数字孪生是真实世界系统的虚拟表现形式。在得到充分实现的情况下,真实系统与虚拟系统之间可以交换信息,从而通过虚拟系统精确地模拟真实系统状态。数字孪生可以使用统计或机理模型来构建。大数据、机器学习和人工智能等统计方法可利用统计数据来预测发展趋势和规律。这些方法可以从数据形式的经验中进行学习。首个获得 QbD 批准的生物制药模型(Gazyva™,Genentech)主要依靠统计建模,例如实验设计 (DoE) (2)。
统计建模的缺点在于,为了捕获系统动力学特征,必须通过数十次,甚至数百次实验来仔细筛选工艺设计空间。此类系统动力学特征一般通过响应面模型捕获,通过该模型建立数字孪生系统,并通过相关训练来应对参数变化问题。相反,由于机理模型根据物理和生物化学原理构建,其本身就能体现这样的系统动力学特征。针对特定工艺进行模型校准时,需要的实验数据更少。因此,对于未经过校准的场景,机理模型也可以对系统动力学特征进行描述,可能不受工艺设计空间限制。所以依托机理模型构建的数字孪生系统可以应对非预期偏倚。
机理模型的内部工作原理
机理建模主要适用于下游工艺(目前已对其物理原理有了深入理解)。层析是其中一个对工艺理解要求较高的应用领域。层析是由多种不同效应叠加的复杂工艺:基本流体动力学、传质现象、相平衡热力学。
图 1 描述了层析柱中的基本作用机制。注入的组分(图 1 中的橙色圆点)在流动相中移动。这种移动可能由不同的作用机制所引起;这些注入的组分在颗粒孔隙外部通过对流和扩散机制传输。对流由连接的泵诱导发生。扩散包括壁效应、分子扩散及其他机制。原料组分可以进入颗粒孔隙内的流动相,之后其移动主要通过扩散实现。最终,组分可以吸附到颗粒的内表面上。
完成层析建模后,还必须考虑组分吸附在吸附球珠内表面的情况。普通模型都是描述吸附物质浓度与颗粒孔隙(或膜上的微孔)中的流动相物质浓度之间的函数关系以及流动相的成分特征(离子强度、pH 值等)。专业模拟软件(如 GoSilico™ 层析建模软件)可以针对离子交换、疏水相互作用和混合模式层析提供各种模型。
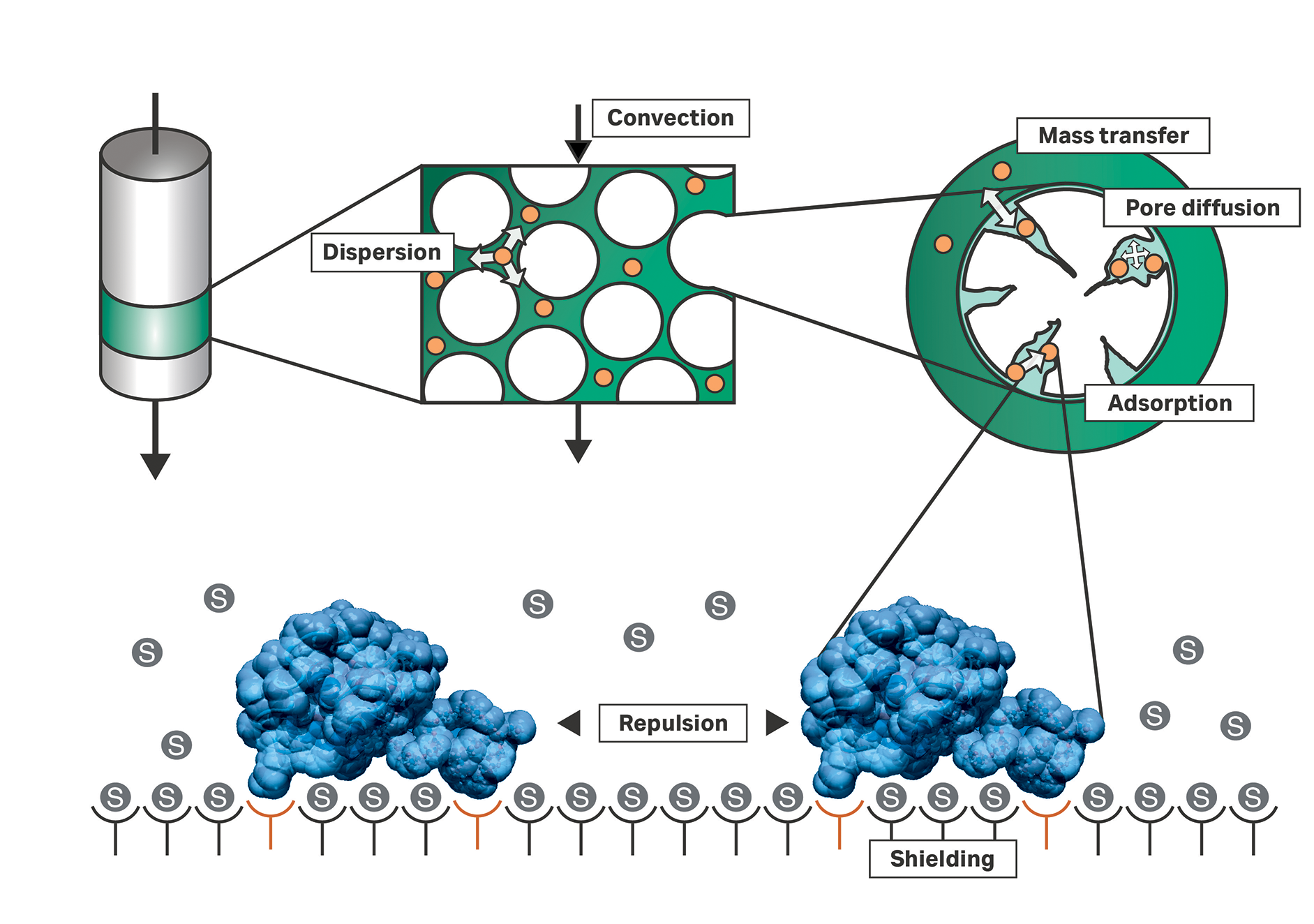
图 1. 层析柱中的基本作用机制。层析图谱是吸附剂颗粒(深绿色)、吸附剂孔隙(浅绿色)和吸附剂表面(白色)之间的空腔中发生的流体动力学和热力学过程的作用结果。不同模型对效应描述的详细程度不同,并可以描述不同的相互作用模式,例如离子交换或疏水相互作用。
构建模型
为了确定模型所研究的效应产生的定量影响,所有层析模型都会包含各种不同的参数。供应商会提供部分模型参数,例如层析柱尺寸和吸附剂平均粒径。许多供应商还会说明材料特性产生的影响。例如,Cytiva 思拓凡提供预表征 f(x) 层析柱,在供货时会提供层析柱的特定详细信息(例如孔隙率和批次的具体填料载量)。
其余蛋白方面的参数需要通过运行校准进行估算。目前,该流程以问题为导向且与相位相适应。对于早期工艺定义,由于可用的样本材料很少,只需通过三次实验即可建立最初模型。通常,如果包含至少一种梯度洗脱,就可以重复使用实验设计 (DoE) 实验。校准一般使用普通的不纯原料进行,并利用数值优化算法进行层析图谱拟合,如图 2 所示。
校准实验的目的不是为了解决分离问题,而是为了理解效应对于层析图谱形状产生的影响,例如传质限制及对于缓冲液成分突然变化的反应。因此,即便是大规模的工艺表征研究,校准实验的次数也很少超过 10 次。简单地说,就是相关物理化学效应的数量是有限的。
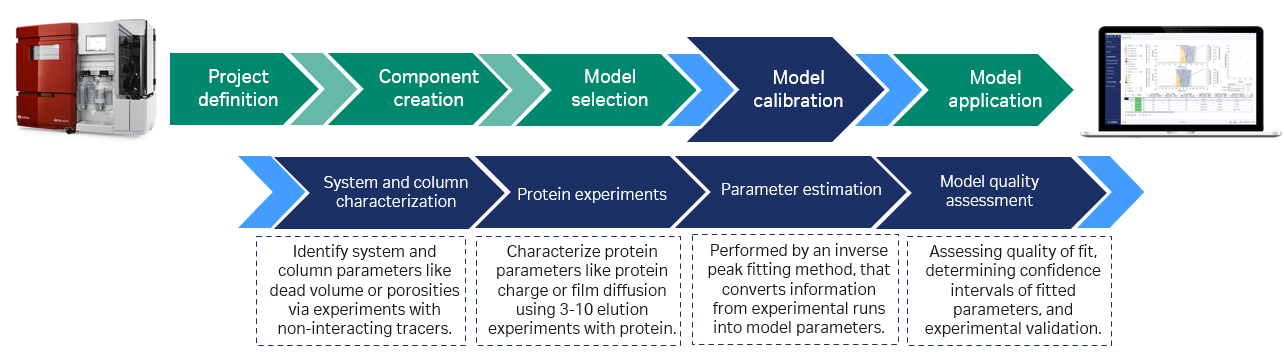
图 2. 建模一般通过示踪法(连接和不连接层析柱)和结合-洗脱法(运行条件接近预期设定值)来完成。然后根据这些实验创建初始模型。可将离线分析获得的其他信息纳入其中。GoSilico™ 层析建模软件通过曲线拟合来估算蛋白质方面的未知模型参数。经过数字模拟优化后,一般会在实验室中再进行一次实验以验证工艺优化情况。
依靠模型进行工艺开发与优化
模拟技术最常见的应用就是对现有工艺进行预测和优化。图 3 所示为使用阴离子交换膜胶囊开发病毒样颗粒纯化步骤。与柱层析法不同的是,流动相泵送时需要通过一个螺旋状膜形成的桶体过滤。在不同的梯度斜率下运行三次梯度洗脱即可建模。仅仅通过计算机优化就可以初步确定两步洗脱工艺,然后通过实验室实验进行验证。由此可以看出,利用工艺建模完全可以设计出具有可选择性、稳健性、可放大性的层析工艺,而且对于复杂原料所需要的实验工作量极少 (3)。
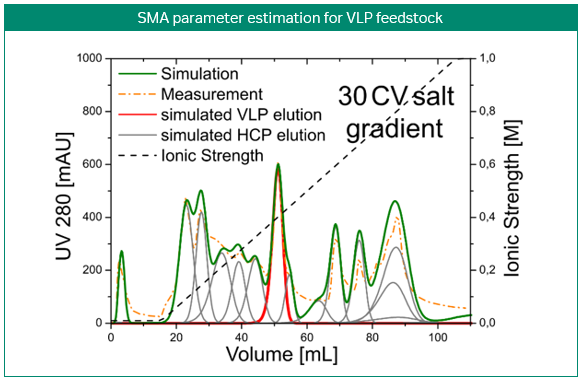
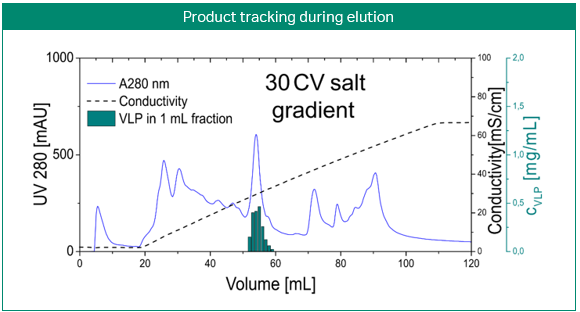
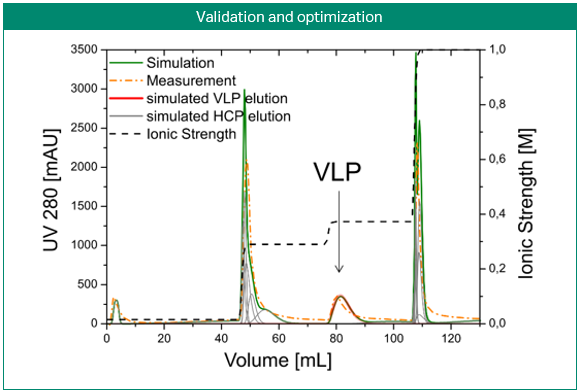
图 3. 使用阴离子交换膜胶囊开发病毒样颗粒纯化步骤。利用模型开发中间洗脱病毒样颗粒(VLP;上部图)捕获步骤。使用 GoSilico™ 层析建模软件校准三次梯度洗脱的空间质量作用 (SMA) 模型(中间图)。使用该模型设计出了两步洗脱工艺并验证成功(底部图)。
分步层析与连续层析之间的连接
生物工艺开发通常需要对各个运行单元进行单独优化。对于采用全面连接的连续化工艺,必须制定整体性的开发策略。在已实现连接的下游工艺中,每个运行单元必须适应之前所有运行工序的工艺与原材料变化。由于传统的实验设计 (DoE) 研究涉及许多关键参数,导致实验工作量剧增,而且造成工艺理解更加困难,因而非常不实用。
而模拟技术又快又经济,不仅可以探索高维度设计空间,而且用时合理。如果有两个或更多运行单元的模型,可以通过数字模拟将它们连接起来,然后作为一个运行单元进行分析或优化即可。这种整体优化方法可以从性能和稳健性方面对连接在一起的工艺进行整体优化。案例研究显示,这种方法对于两步式连续性离子交换层析工艺的优化具有优越性 (4)。有作者表示,单独对每个运行单元进行优化,可导致整体工艺表现欠佳。
单层析柱与多层析柱装置的物理原理相同,因此机理模型还可以作为一种策略将分批运行建模转为连续运行建模。我们可以通过数字模拟对连续层析的多层析柱装置进行评估,确定最优工艺条件,从而评估并优化系统达到稳态运行所需的时间。
工艺放大与缩小
我们也可以利用计算机模型进行数字模拟,将实验室工艺放大为试点规模、甚至生产规模的工艺。该数字模拟层析工艺放大与缩小的基本前提条件是只有孔隙系统外部的流体动力学发生变化;假定孔隙系统内部的效应与规模变化无关。样本组分进入孔隙系统后,无论是在滤板中装填的吸附球珠内还是在生产层析柱中,扩散、吸附、解吸都遵循同样的机制。案例研究表明,热力学特性与规模大小无关 (5)。我们只需要知道基本的流体动力学特性就可以对新规模的整个工艺进行预测,而通过层析柱鉴定运行等方法即可获得流体动力学特性。这在一定程度上改变了作为小规模模型的小型层析柱的处理方法。目前认为,层析图谱的一些特性(例如峰展宽,甚至最终的质量属性)与工艺规模有关。通过模型可以理解不同规模的差异,从而帮助实现不同规模的转换。
模拟可以提供解决方案
随着层析建模工具的不断发展,这种技术已具备经济高效的计算机模拟功能,可以节省时间与成本,因此已经可以取代实验室实验。其建立模型需要的实验室实验数量少,模拟时间短,因此各项开发活动可以同步开展。由于采用了第一性原理模型,我们可以通过模型理解相关工艺,从而在工艺设计空间与产品质量之间建立了联系。可以提前预测和纠正后续单元运行问题。因此,发展完善的数字孪生技术有望在未来的原材料变化处理、批次控制及实时放行测试方面发挥重要作用。
参考文献
- EMA. Questions and answers on design space verification. EMA/603905/2013 24 October 2013. https://www.ema.europa.eu/en/documents/other/questions-answers-design-space-verification_en.pdf.
- Kelly B. Quality by Design risk assessments supporting approved antibody products. mAbs 2016; 8(8): 1435-1436.
- Effio CL, Hahn T, Seiler J et al. Modeling and simulation of anion-exchange membrane chromatography for purification of Sf9 insect cell-derived virus-like particles. Chromatogr A. 2016;1(429): 142-154.
- Huuk TC, Hahn Y, Osberghaus A, Hubbuch J. Model-based integrated optimization and evaluation of a multi-step ion exchange chromatography. Sep. Purif. Technol. 2014; 136:207-222.
- Huuk, T, Hahn T, Griesbach J, Hepbildikler S, Hubbuch J. Scalability of mechanistic models for ion exchange chromatography under high load conditions in Extended reports: High-throughput Process Development.10–13. Cytiva. CY13184-11Dec20-BR. 2020.