随着 Kymriah™ 和 Yescarta™ 等自体嵌合抗原受体 (CAR) T 细胞疗法的推出,细胞疗法在美国和欧洲首次亮相。
全球目前有 250 多项临床试验来研究 CAR T - 细胞疗法,其他细胞疗法也在开发中,潜在的适应症扩大到包括恶性肿瘤(比如黑色素瘤、胰腺癌和胶质母细胞瘤)在内的实体肿瘤。此外,研究人员还在研究干细胞疗法,以治疗自身免疫性疾病、阿尔茨海默氏症和帕金森氏症等疾病。
然而,细胞疗法的成功不仅在于一种产品可以发挥预期内的治疗效果,更在于如何克服生产过程中的重重挑战并最终实现病人的回输。为了积极应对这些供应链的挑战,并成功实现细胞疗法的商业化生产,企业需要灵活应用杰出的技术和创新的策略。
细胞疗法初期的商业化发展主要聚焦在临床效果上。在这个快速发展的过程中,企业没有时间去打造强大的、可放大的生产工艺。虽然商业化产品已经成功上市,但是自动化的缺乏、供应链的不成熟、过时的分析体系等生产过程的问题都在涌现出来。
现在,行业认识到需要扩大细胞疗法的生产规模以满足巨大的需求,因此正在努力实现流程工业化,并更好地纳入供应链考虑因素。
细胞疗法的生产需要创新的模式
在传统的生产操作中,工艺往往受限于固化的生产设施中。但对于细胞疗法,远不止此,因而也带来了其独特的物流运输的挑战与对应的企业责任。这些都需要细胞治疗的企业通过转变思维模式来实现创新生产。
细胞疗法生产以临床(或单采)机构从患者身上采集细胞开始,以对患者使用最终药物产品结束。
从原材料的初始收集到产品的最终使用,需要经过几十道交接点和工艺。供应链中所有这些活动环节的复杂性,以及生产和使用阶段的融合代表了一个新的领域,也是细胞疗法领域与传统制药行业的区别所在。
成功的供应链需要完成映射整个生产过程。生产商必须要了解关键交接点在哪里,并了解每一步的风险。
一旦所有关键步骤的全面路线路就位,就必须纳入风险缓解策略,特别是要引入自动化。由于自体细胞疗法是批量定制的个性化产品,因此在整个制造供应链中,无论多么复杂,生产商还必须确保维持监管链和同一性。
未记录和控制样本的来源可能会给患者带来可怕甚至致命的后果。谨慎追踪还确保了医生和生产团队的一致性、稳健性以及质量控制。
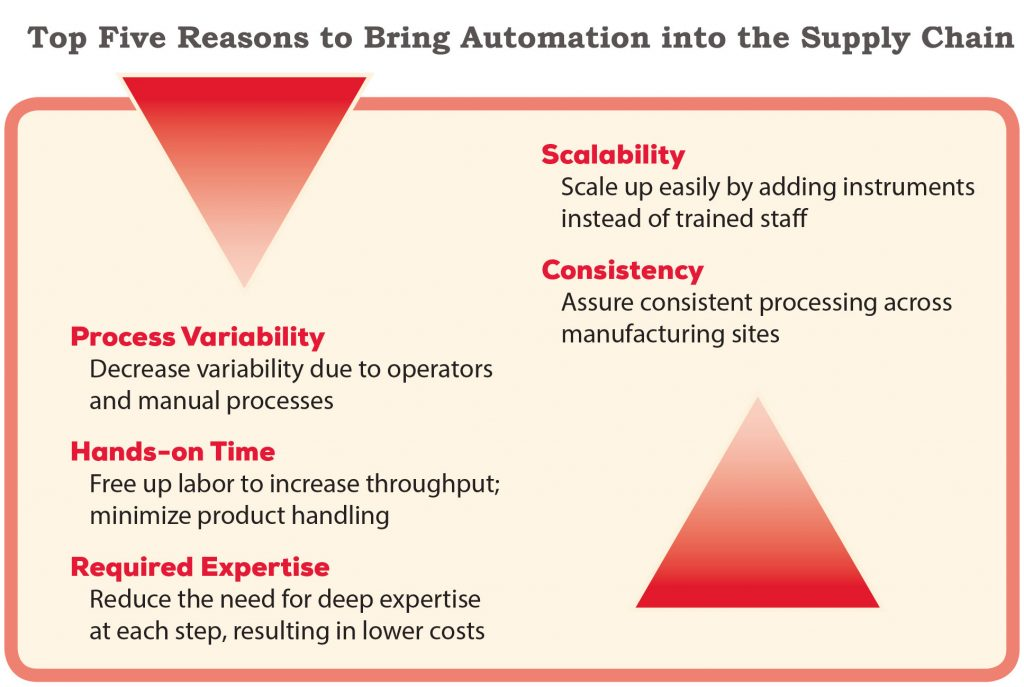
自体细胞治疗产品各有特点,因此需要自动化,目的是降低工艺可变性并提高可扩展性。
除物流方面的挑战之外,细胞疗法生产商还必须使用变化多样的起始材料来生产安全、有效的产品。通常提供原材料的患者(如自体细胞疗法)具有不同的遗传背景、疾病阶段和病史,它们会使上游生产工艺更加复杂和多变。
换言之,起始材料每次都不一样,与典型的生产场景有很大的不同,因为在典型的生产场景中,每次生产都使用明确的细胞系。“归根结底在于所涉及的系统十分复杂,我们使用的是活的起始材料和产出活的产品”,Cytiva 全球研发主管兼细胞与基因疗法总监 Aaron Dulgar-Tulloch 博士说。
"这意味着随供体和细胞状况的变化,前端也会变,”Dulgar-Tulloch 博士继续说道。
增强自动化以扩大规模
即便不是全部,大多数市售的细胞疗法也都是针对少数患者人群。如果要在多种适应症中广泛使用这些治疗方法,就需要在自动化、工艺简化和供应链管理方面进行改进,以满足需求。
为了扩大规模,生产工艺必须从开放和手动转变为封闭和自动化,减少污染和降低风险,提高产品一致性和效率,并在整个工艺中增加可追溯性,以确保监管链。
随着自动化程度的提高,操作员可以在关键工艺步骤中测量关键产品属性,以更好地控制起始材料的可变性。工业界和学术界的团体已经在采用新技术,开发自动化、封闭性和可放大性更高的系统,从而消除风险并为未来产量的增加做好准备。
由于存在很大的可变性风险,自动化对于生产单剂量的自体细胞疗法产品尤为关键。因此,生产商在工艺开发中投入时间在关键步骤实现自动化来消除人工交互过程中的误差,可以使企业大大获益。
引入自动化体系的时机也很重要——要在适当的时间将自动化引入临床开发或者研究平台。如果过早引入,问题可能会进一步出现;但是引进太晚,就可能出现重复劳动,重复研究,因为要向监管机构证明引入自动化设备不会改变产品的质量。
外包供应链
对于不熟悉工艺的公司来说,建立一个完备且强大的生产供应体系可能既困难又耗时。
对于那些在产品生物学方面拥有深厚专业知识,但是不知道如何从小型手动工艺转变为规模化、自动化生产,进而满足全球数万至数十万患者需求的公司而言,合同制造组织 (CMO) 或 Cytiva 等外部团队可以帮助他们迅速缩小差距。
这些组织机构了解客户需要进行哪些类型的实验,以及如何进行这些实验,以便将学术或转化规模的工艺转化为商业化的工艺。CMO 也可以帮助选择适当的设备。外包也有助于生产商规避大规模系统和设施的投资风险。以免产品延迟上市或未通过监管的批准而蒙受巨大损失。
如果一家企业决定外包,则应努力了解工艺决策,以便以后选择将工艺带回内部。
“不要把你的产品开发交给别人,而自己却几乎不参与其中”,Dulgar-Tulloch 博士说。”否则,企业很快就会发现自己任 CMO 摆布,因为所有产品生产专业知识都掌握在 CMO 手中。”
至于什么时候开始考虑供应链和外包选项,Dulgar-Tulloch 博士的建议是尽早开始。如果一家企业一直等到产品准备好再上市销售,当他们试图赶上或希望改变限制条件时,将面临“巨大的”延迟和挫折。
采用我们的细胞和基因治疗方案,消除疗法上市路上的障碍。